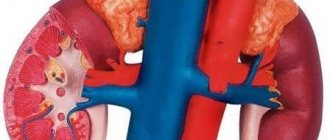
Гиперандрогения у женщин – патологическое изменение гормонального фона, проявляющееся в излишней выработке в организме половых гормонов мужчины — андрогенов. Это распространенное заболевание эндокринной системы, которым страдает около 5% представительниц прекрасного пола. В норме андрогены в небольшом количестве обязательно присутствуют в организме каждой женщины. Они необходимы для нормального полового созревания, работы печени, почек, здоровья репродуктивной системы. Мужские половые гормоны участвуют в синтезе эстрогена, который, в свою очередь, способствует сохранению крепких костей женщины в зрелом возрасте.
Чрезмерное андрогенов в женском организме – патология, требующая обязательной медицинской коррекции. Без своевременного выявления симптомов и лечения со временем возникают необратимые тяжелые изменения в организме. Но оно может быть адекватным, только если правильно определена причина, которая вызвала этот недуг. Это обусловлено тем, что универсальной терапии гиперандрогении не существует, ее способы напрямую зависят от факторов, повлиявших на развитие патологии.
Немного о генетике
Многие болезни относятся к рецессивным и проявляют себя только при встрече двух одинаковых генов, то есть, в гомозиготном состоянии, в то время как гетерозиготы остаются здоровыми и даже не подозревают, что являются носителями наследственной патологии. Однако гены не оказались стабильными на 100%, поэтому генетика – наука не только о наследственности, но и об изменчивости.
Гены, хоть и не так часто, но меняются, и это явление, называемое мутацией, находит свое отражение в изменении признаков организма.
Мутагенез (мутационный процесс), в общем-то, считается процессом случайным, но доказано, что некоторые факторы все-таки способны на него повлиять. К ним относятся:
- жесткое излучение, например, рентгеновские лучи;
- химические вещества, обладающие мутагенными свойствами;
- генетически модифицированные продукты питания;
- стрессы, психо-эмоциональные нагрузки;
- неадекватное лечение гормональными препаратами;
- инфекционно-вирусные агенты.
Обмен любых веществ в организме складывается из двух, идущих параллельно, но сопряженных между собой ферментативных процессов:
- расщепления сложных соединений до простых молекул (катаболизм);
- синтеза сложных веществ, предшественниками которых являются простые молекулы (анаболизм).
В метаболических превращениях продуктов обмена участвуют тысячи ферментов, каждый их которых должен отвечать за свой участок и безупречно выполнять свою работу. Однако в результате генетических мутаций, фермент может изменить свой состав и свойства, то есть, стать дефектным и потерять способность справляться с назначенной природой задачей. Мутации генов, кодирующих ферменты, отвечающие за биосинтез и функционирование таких важных для организма веществ, как гормоны, приводят к эндокринным дефектам, затрагивающим продукцию и транспорт половых гормонов.
Мутации генов, контролирующих синтез андрогенов, бесследно не проходят и приводят к патологическому состоянию, называемому адреногенитальным синдромом (АГС) или адреналовой гиперплазией (гиперплазия коры надпочечников).
Почему болит низ живота у женщин? Это может носить просто физиологический характер, но при этом, подобного рода симптомы присутствуют и у большого количества женских заболеваний. Поэтому, если боль есть, обязательно надо определить причину ее возникновения.
Понять из-за чего возникает внематочная беременность и как ее избежать, вам поможет информацию из этого источника
Общие сведения
Вирилизация (маскулинизация) надпочечникового генеза обуславливается чрезмерным продуцированием надпочечниками гормонов андрогенного типа и приводит к внешним и внутренним изменениям, атипичным для пола пациента. Андрогены необходимы в организме взрослой женщины, поскольку отвечают за важные преобразования организма в процессе полового созревания. В частности, они производят синтез эстрогена, а также способствуют укреплению костной ткани, росту мышц, участвуют в регуляции работы печени и почек и формировании репродуктивной системы. Производятся андрогены в основном надпочечниками и в женском организме яичниками, а в мужском, соответственно, яичками. Существенное превышение нормы содержания этих гормонов у женщин способно значительно расстроить репродуктивную систему и даже спровоцировать бесплодие.
Типы АГС
Клинические проявления и свойственные им биохимические показатели позволяют разделить адреногенитальный синдром на пять основных типов.
I. Редко встречающаяся липидная адреналовая гиперплазия, при которой блокада стероидогенеза возникает еще на начальных стадиях, до образования ферментов, расщепляющих холестерин. В результате этого холестерин накапливается в надпочечниках, а АКТГ (адренокортикотропный гормон) – в крови. Клинически этот тип проявляется выраженной вирилизацией у девочек, гипоспадией (врожденный порок развития мочеиспускательного канала) и аномалией мошонки у мальчиков. Потеря с мочой хлоридов характерна для обоих полов.
II. Биохимическую основу АГС этого типа составляет недостаточное содержание фермента 3β-ол-дегидрогеназы, который обеспечивает синтез прогестерона. В итоге: у мальчиков проявление феминизации, так как нарушен синтез стероидов с андрогенным действием.
III. К этому типу, возникающему ввиду недостаточности фермента 2-гидроксилазы, относится подавляющее большинство больных с АГС (почти 90%). Две основные формы адреногенитального синдрома (простая и сольтеряющая) формируются в зависимости от концентрации 21-гидроксилазы, где при частичной форме вирилизация у девочек происходит еще до рождения, а половое созревание наступает со значительным опозданием. Мальчикам, этот тип, наоборот, грозит преждевременным половым созреванием, сочетающимся с низкорослостью.
Полная утрата активности фермента приводит к тяжелым и ранним проявлениям синдрома:
- пилороспазму;
- потере солей;
- метаболическому ацидозу;
- приступам коллоптоидного состояния;
- изменениям биохимических показателей крови и мочи (гормональные сдвиги, соответствующие блокаде).
IV. Клиническая картина этого типа обусловлена блокадой превращения 11-дезоксикортизола в кортизол (снижение уровня 11β-гидроксилазы) и, помимо вирилизации и у мальчиков, и у девочек, проявляется прогрессирующей артериальной гипертензией, характеризуемой:
- изменением сосудов почек и глазного дна;
- гипертрофией сердечной мышцы;
- задержкой в организме соли (NaCl);
- выделением повышенного количества 11-дезоксикортизола с мочой.
V. Очень редкий тип адреногенитального синдрома. Встречается, когда мутационная блокада затронула стадии превращения прогестерона в 17α-гидроксипрогестерон.
Артериальная гипертензия, свойственная IV типу, вовсю начинает развиваться уже в детском возрасте, к тому же плохо поддается лечению.
Причины патологии
Что такое – гиперандрогения и почему она возникает? Основными причинами заболевания являются:
- опухоли, метастазы надпочечников;
- нарушение гипоталамо-гипофизарной регуляции, вызванное травмами, опухолями, воспалительными заболеваниями головного мозга;
- опухоли яичников: лютеома, текома;
- андрогенитальный синдром – врожденная патология коры надпочечников, при которой происходит усиленная выработка тестостерона.
У женщин причины гиперандрогении вызывают нарушение гормонального баланса, функционирования репродуктивной системы, метаболических процессов в организме.
Механизм формирования
Синтез андрогенов (мужских половых гормонов) происходит в яичках и надпочечниках. Этот процесс на начальных этапах идет одинаково в обоих органах и является общим для андрогенов и других стероидов, вырабатываемых надпочечниками: кортизона, кортикостерона и альдостерона. Основными ферментами, которые обслуживают ступени последовательных превращений предшественников тестостерона, являются гидроксилазы и дегидрогеназы.
Казалось бы, раз дело касается мужских половых гормонов, то и патология должна быть присуща только мальчикам, однако это не так, поскольку на начальных этапах биосинтез эстрогенов (женских половых гормонов) ничем не отличается от такового у мужчин, поэтому эти мутации также возможны и у индивида женского пола.
И когда у девочки проявляются черты противоположного пола, принято говорить об адреногенитальном синдроме, который может быть представлен тремя клиническими формами:
- врожденной;
- постнатальной или препубертатной;
- постпубертатной.
Гормональные сдвиги вызывают нарушение половой дифференцировки, которое нередко берет начало еще во внутриутробном периоде, а затем продолжается в постнатальном. Разумеется, если адреногенитальный синдром проявляется уже у новорожденных, то вряд ли можно подвергать сомнению его врожденную наследственную природу. Такую форму гиперандрогении называют классической, и она часто ставит в затруднительное положение неонатологов при определении пола ребенка.
Полезное видео
О лечении и диагностике гиперандрогении у женщин смотрите в этом видео:
Похожие статьи
- Синдром поликистозных яичников: причины, симптомы…
Слышит диагноз синдром поликистозных яичников (СПКЯ) каждая десятая девушка. Причины кроются в гормональных сбоях. Симптомы — сбои в месячных циклах, бесплодие. УЗИ и другие методы диагностики помогают подтвердить диагноз, чтобы начать лечение. Читать далее - Синдром истощения яичников: основные причины…
Определяют синдром истощения яичников даже у очень молодых девушек. Причины могут крыться в наследственности, гормональных нарушениях. Иногда называют ранний климакс, хотя преждевременное истощение яичников — это не совсем то. Без лечения забеременеть невозможно, иногда спасает только ЭКО. Читать далее
- Альгодисменорея: лечение, причины первичной…
Если выявлена у девочек альгодисменорея, лечение необходимо начать как можно скорее. Она бывает первичной и вторичной, подросткам ставят зачастую диагноз «синдром НМЦ по типу», женщинам — вторичную. Симптомы — острая боль при месячных, изменения эмоционального фона. Помогут препараты, таблетки, ЛФК. Читать далее
- Дисфункция яичников: признаки, причины…
Возникает дисфункция яичников в совершенно любом возрасте — у подростков, в репродуктивном, бывает климактерическая. Причины могут быть как природные, внутренние, внешние. Лечение длительно, успех зависит от своевременности обращения к врачу. Читать далее
Врожденная адреналовая гиперандрогения
Начавшаяся еще во внутриутробном периоде избыточная продукция андрогенов неизбежно приводит к гиперплазии коры надпочечников и формированию ложного гермафродитизма. А так как пол первоначально определяют по наружным половым признакам, то наличие пенисообразного клитора и слившихся лабиосакральных складок, напоминающих мошонку, заставляют думать о принадлежности ребенка к мужскому полу.
Врожденный адреногенитальный синдром принадлежит к наследственным дефектам и передается по аутосомно-рецессивному типу. Обусловлен он врожденной недостаточностью ферментных систем и, в частности, 21-гидроксилазы, контролирующей синтез глюкокортикоидов в коре надпочечников. Если недостаток 21-гидроксилазы незначительный, то говорят о простой форме АГС, но в случае глубокого дефицита фермента развивается тяжелая форма синдрома. Это происходит вследствие недостатка кортизола и альдостерона, которые не могут синтезироваться ввиду несостоятельности коры надпочечников, а вернее, ее гиперплазии, что приводит к постоянной потере солей организмом, поэтому такой вариант адреногенитального синдрома называется сольтеряющей формой.
Кроме того, избыточное количество андрогенов существенно влияет на формирование наружных половых органов и влечет развитие у девочек ложного мужского гермафродитизма разной степени выраженности, который на ранних стадиях врожденного АГС проявляется неправильным формированием скелета с преобладанием мужских черт.
Следует заметить, что суммарная частота такой гиперандрогении довольно высока и встречается в гомозиготном состоянии в соотношении 1 : 5000-10000, в гетерозиготном – приблизительно 1 : 50.
Врожденный адреногенитальный синдром, помимо нарушения половой дифференцировки еще до рождения ребенка, чаще других видов гиперандрогений характеризуется расстройством минерального обмена и другими тяжелыми нарушениями.
Надпочечниковая гиперандрогения
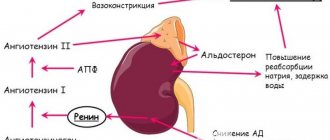
Несмотря на то, что адреногенитальный синдром включает несколько форм, общим для всех является задержка продукции кортизола в надпочечниках, влекущая стимуляцию выработки адренокортикотропного гормона (АКТГ) гипофизом, что в свою очередь стимулирует синтез 17-гидроксипрогестерона и ведет к гиперпродукции андрогенов. Накопление в крови АКТГ приводит к снижению уровня кортизола и увеличению выделения с мочой 17-кетостероидов или 17-гидроксикортикостероидов. Эти показатели являются очень важными диагностическими признаками и успешно используются для установления диагноза АГС. Но коль все эти превращения завязаны на коре надпочечников, то такой АГС называют гиперандрогенией надпочечникового генеза, которая, кроме врожденной формы, имеет (как сказано выше) еще две: постнатальную и постпубертатную. Они не всегда являются врожденными, так как могут развиваться вследствие гиперплазии коры надпочечников, возникающей по различным причинам, или образования опухоли, что случается значительно реже.
Постнатальная(препубертатная) форма АГС характеризуется ранним половым созреванием и имеет следующие признаки:
- вирилизация ( рост волосяного покрова на лице и теле по мужскому типу, увеличение клитора, огрубение голоса);
- наличие многочисленных розовых угрей на лице, груди и спине;
- усиленный рост костей (до наступления менархе девочки с препубертатной формой значительно опережают ровесниц);
- раннее закрытие эпифизарных зон хрящей, поэтому рост прекращается и дети, в конечном итоге, остаются низкорослыми. Типичными для синдрома являются короткие нижние конечности.
Клиническая картина постпубертатной формы АГС характеризуется:
- вириальным синдромом;
- признаками дефеминизации (уменьшаются молочные железы, наступает гипо- или аменорея);
- гирсутизмом (огрубевает голос);
- увеличением клитора.
Очевидно, что предположить диагноз можно и по внешнему виду человека, к тому же, все эти нарушения хорошо отражаются в крови и моче, поэтому диагностика адреногенитального синдрома особых проблем не составляет. Диагноз ставится на основании:
- клинической симптоматики;
- общего осмотра;
- гинекологических исследований;
- исследования гормонального статуса (венозная кровь) с помощью иммуноферментного анализа;
- биохимического анализа мочи (17-кетостероидов, 17-оксикортикостероидов).
Адреногенитальный синдром, естественно, влияет на репродуктивную функцию и ставит под сомнение наступление беременности, однако существуют и другие виды гиперандрогений, которые следует различать, так как они чаще, чем АГС, приводят к бесплодию. Например, яичниковая гиперандрогения или надпочечниковая и яичниковая одновременно.
Симптомы
Надпочечниковая гиперандрогения у большинства женщин проявляется целой плеядой специфических симптомов. Все клинические признаки условно разделяют на две категории: основные и второстепенные.
- Чрезмерное оволосение кожных покровов. Рост волосяного покрова, в первую очередь, наблюдается в районе живота (особенно в нижнем сегменте), груди, верхних и нижних конечностей. Самая тяжелая форма – гирсутизм – на щеках женщин начинают расти грубые волосы;
- Появление характерных залысин на голове (алопеция адреналового генеза у женщин);
- Сильные изменение состояние дермального полотна (формируют угри, акне, прыщи, шелушения, воспалительные реакции). Важный нюанс – любые манипуляции со стороны косметолога не дают никаких результатов, так как причина кроется глубоко внутри;
- Мышечная атрофия;
- Стремительное развитие остеопороза.
Синдром гиперандрогении могут формировать самые различные патологические процессы: гипертрофия надпочечников, травмы гипоталамуса, дисфункция любой железы в организме, многое другое. В зависимости от того, какие причины лежат в основе заболевания, как сильно они повлияли на пациентку, и будет зависеть течение заболевания и наличие второстепенных симптомов. Женщины могут страдать от таких аномальных явлений и патологических состояний:
- Резкий набор веса;
- Формирование половых органов по промежуточному типу;
- Аномалии менструального цикла;
- Бесплодие (реже – невынашивание плода, так как женщине в принципе трудно забеременеть);
- Резкие скачки артериального давления;
- Себорея;
- Барифония (резкое огрубение и понижение тональности голоса).
Женщины склонны к депрессивным состояниям. Они чаще простуживаются, быстрее утомляются.
Гиперандрогения смешанного генеза
Гиперандрогения яичникового генеза, имеющая название «поликистозных яичников» (ПКЯ), очень часто является причиной привычных выкидышей и бесплодия. Структурные и функциональные изменения яичников, происходящие на фоне нейрообменных патологических процессов, обусловлены расстройствами гипоталамо-гипофизарного отдела нервной системы. Причиной яичниковой гиперандрогении является функциональные нарушения активности гипоталамических структур, которые, начиная с пубертатного периода, должны регулировать выделение рилизинг-гормон лютеинизирующего гормона (РГЛГ). Но поскольку данная патология характеризуется усиленным выделением и выбросом РГЛГ, это приводит к хронической ановуляции (отсутствие овуляции), возникающей вследствие нарушений:
- фолликулогенеза;
- синтеза стероидов в яичниках;
- метаболизма.
Так как эти расстройства начались в пубертатном возрасте, то главным симптомом заболевания становится первичное бесплодие, хотя имеют место и другие немаловажные для диагностики проявления болезни:
- увеличение яичников;
- олигоаменорея (менструальный цикл удлиняется до 40 дней и более, кровотечения незначительны) или ациклические кровотечения (реже);
- увеличение массы тела;
- гипертрихоз (чрезмерный рост волос).
Следует заметить, что яичниковая гиперандрогения может сочетаться с надпочечниковой, то есть, две эти формы могут встречаться одновременно у одной женщины. Такая патология также обусловлена гипоталамическими и нейроэндокринными расстройствами, но в формировании гиперандрогении смешанного генеза немалую роль играют обменные нарушения кортизола и инсулина, то есть, надпочечники в данном случае принимают самое активное участие. Гиперандрогению смешанного генеза, в основном связывают с наличием генетического дефекта 3α-гидроксистероиддегидрогеназы, приводящего к накоплению дегидроэпиандростерона, который подвергается дальнейшим превращениям. Результатом их становится избыточное содержание андрогенов в тканях организма женщины.
Вызванный патологическими процессами гормональный дисбаланс, проявляется неадекватным функционированием и других эндокринных органов, например, вегетативно-невротические расстройства зачастую сопровождаются неправильным поведением щитовидной железы. Поскольку в данном процессе задействован инсулин, то и поджелудочная железа не может остаться в стороне.
Происходящие в организме превращения приводят к значительному нарушению гормонального равновесия и дисфункции эндокринной системы. Это влечет за собой не только изменение внешнего вида женщины (приобретение мужских черт), но и выливается в тяжелые гормональные заболевания, которые препятствуют наступлению и вынашиванию беременности.
Отсутствие практики обязательного генетического анализа после замершей беременности, приводит к тому, что причины замирания, как правило, остаются неизвестными.
О механизме действия, основных методах и эффективности экстренной контрацепции и связанных с ней рисках далее
Какие показания к применению и как правильно принимать метронидазол, можно узнать перейдя по этой ссылке /metronidazol
Особенности развития адреногенитального синдрома у женщин
Адреногенитальный синдром у женщин приводит к серьезным изменениям в функционировании яичников и нарушениям в репродуктивной системе. Согласно статистическим исследованиям, каждая пятая женщина в той или иной степени страдает гиперандрогенией с различными проявлениями. Причем возраст в данном случае не имеет значения, заболевание проявляется на любом этапе жизненного цикла, начиная с младенчества.
Воздействие гиперандрогении на функцию яичников вызывает следующие проявления:
- угнетение роста и развития фолликулов в ранней фазе фолликулогенеза проявляется аменореей (отсутствием менструаций в течение нескольких циклов);
- замедление роста и развития фолликула и яйцеклетки, не способной к овуляции, способно проявиться ановуляцией (отсутствием овуляции) и олигоменореей (увеличением интервала между менструациями);
- овуляция с дефектным желтым телом, выражается в недостаточности лютеиновой фазы цикла, даже при регулярных менструациях.
Вернуться к оглавлению
Лечение надпочечниковой гиперандрогении
Учитывая наличие различных форм гиперандрогении и тесную связь эндокринных нарушений со всеми системами организма, лечить заболевание весьма сложно.Корригирование дисбаланса осуществляется назначением и индивидуальным подбором гормональных препаратов с учетом происхождения и степени гиперандрогении, поэтому лечение народными средствами без участия врача вряд ли уместно. Правда, для некоторой коррекции гормонального фона прибегают к использованию средств нетрадиционной медицины – гомеопатическим препаратам растительного происхождения, которые, однако, следует отличать от приготовленных в домашних условиях настоек и отваров. Применение антиандрогенов растительного происхождения вполне допустимо и оправдано в адекватных дозах и при определенных, не требующих корректировки их синтетическими аналогами, проблемах.
Лечение врожденной формы адреногенитального синдрома должно быть начато как можно раньше, учитывая то, что мускулинизация скелета, которая была приобретена за время болезни, уже никуда не денется, то есть, устранить ее постфактум невозможно. Раннее начало лечения способно спасти и от многих других неприятностей.
Врожденная форма адреногенитального синдрома часто является причиной неправильной сексуальной ориентации и требует в дальнейшем изменения «паспортного» пола, что очень болезненно воспринимается самим человеком и дает почву для осуждения его поведения невежественным в этом вопросе людьми.
Надпочечниковая гиперандрогения лечиться длительно (от одного года да 15-ти). В течение этих лет больной регулярно получает подобранные индивидуально дозы глюкокортикостероидных препаратов, подавляющих синтез многих половых гормонов в надпочечниках. Обязательно во время лечения проводится контроль 17-кетостероидов, выделяемых суточной мочой. Глюкокортикоидную заместительную терапию проводят и больным с постнатальной и постпубертатной формами АГС, однако лечение здесь начинается с больших доз гормонов (15-20мг преднизолона или 2 мг дексаметазона в сутки в течение недели) под постоянным контролем 17-кетостероидов в суточной моче. После 7 дней приема стероидов, дозу начинают постепенно снижать, доводя ее до поддерживающей. Как только нормализуется показатель 17-кетостероидов и отрегулируется менструальный цикл, дозы препаратов пересматриваются. В таких случаях обычно оставляют прием глюкокортикостероидов только в первой фазе менструального цикла.
Диагностические мероприятия
В самом начале врач должен провести дифференциальную диагностику, исключив другие специфические заболевания. Речь идет о следующих патологиях:
- Акромегалия;
- Печеночные недуги;
- Аномальная дифференциация по половому признаку;
- Синдром Кушинга;
- Опухолевые образования надпочечников, способные секретировать андрогены.
Диагноз надпочечниковая гиперандрогения может быть поставлен только после всех надлежащих диагностических процедур. В первую очередь, пациентка назначают следующие анализы:
- Изучение гормонального фона. Современные методы обследования в лаборатории позволяют точно выяснить количество пролактина, свободного и общего тестостерона, уровня ФСГ в крови. Из-за того, что гормональные вещества в течение суток вырабатываются неравномерно, пробы делают трижды на сутки;
- Идентификация кетостероидов в моче;
- Маркеры на ХГ.
Лечение поликистозных яичников и гиперандрогении смешанного генеза
Яичниковую гиперандрогению можно лечить и консервативным путем, и хирургическим.
Целью консервативной терапии первичных поликистозов яичника является:
- стимуляция овуляции (лечение бесплодия);
- профилактика гиперплазии эндометрия.
Назначение комбинированных эстроген-гестагенных препаратов (комбинированные оральные контрацептивы – КОК) для подавления роста концентрации гонадотропинов и торможения пролиферативных процессов в эндометрии. Однако известный препарат (КОК) Диане-25, обладающий антиандрогенным эффектом, назначают только в случае, если женщина не планирует беременность. Другие варианты требуют и другого подхода (назначение глюкокортикоидов в малых дозах).
Оперативное лечение ПКЯ можно осуществлять с помощью нескольких методов:
- клиновидной резекции яичников;
- демедуляцией яичников с надсечкой (или без нее) фолликулярных кист;
- электрокаутеризацией;
- термокаутеризацией.
Последние два способа являются альтернативой клиновидной резекции яичников и осуществляются лапароскопическим методом.
Труднее всего лечить гиперандрогению смешанного генеза, особенно, если женщина планирует беременность. В таких случаях в течение года обычно принимают малые дозы дексаметазона для подавления выработки дегидроэпиандростерона в надпочечниках. При этом контролируют содержание кортизола в крови больной, который никак не должен превышать показатель в 5мкг%.
По истечении года гормональный статус женщины подлежит всестороннему исследованию и, если обнаруживается, что подавляющее большинство андрогенов производится не надпочечниками, а яичниками, лечебную тактику меняют и назначают комбинированные оральные контрацептивы (тоже в малых дозах).
Есть и другие схемы лечения гиперандрогении, которые используются врачом после установления формы, происхождения и степени выраженности клинических проявлений заболевания.
Всегда следует иметь в виду, что даже малые дозы глюкокортикостероидных препаратов способны привести к развитию синдрома Кушинга,поэтому индивидуальный подбор дозы и исследование гормонов 1 раз в месяц при проведении терапии являются обязательными мероприятиями.
Симптоматика
Различают три направления развития симптомов:
- Косметические дефекты
- Гинекологические заболевания
- Нарушение обмена веществ
- Акне
- Нарушение менструального цикла
- Сахарный диабет II типа
- Себорея
- Ановуляция
- Ожирение верхней части туловища
- Гирсутизмия
- Бесплодие
- Гиперлипопротеинемия
- Алопеция
- Гиперплазия эндометрия
- ПКЯ
Препараты-антиандрогены
Половые гормоны – вещь очень тонкая и трудноуправляемая. При их снижении у мужчин наступают нежелательные сексуальные расстройства, например, такие как импотенция и снижение полового влечения.
У женщин избыток мужских половых гормонов приводит к усиленному росту волос на лице, но выпадению на волосистой части головы, уменьшаются молочные железы, меняется голос, нарушается менструальный цикл. С целью подавить выработку мужских половых гормонов и снизить их концентрацию, (следовательно, и активность) в сыворотке крови при гиперандрогении назначают препараты-антиандрогены, которыми, как правило, являются оральные контрацептивы. Однако, учитывая, что список их и приведенные схемы лечения, могут быть восприняты некоторыми читателями, как руководство к действию, останавливаться подробно на этой группе нет никакого смысла, хотя познакомиться поближе с антиандрогенами растительного происхождения не будет лишним. Тем более, что некоторые косметические средства в своих составах их имеют, да и в климактерическом периоде многим женщинам они очень помогают.
Такое вещество, как Saw Palmetto, основой которого является экстракт карликовой пальмы, входит в состав лекарственного средства от облысения Ринфалтил.
Цимифуга (клопогон) известна женщинам «бальзаковского возраста», так как входит в состав многих растительных препаратов, предназначенных для борьбы с неприятными проявлениями климактерического периода. При гормональном дисбалансе часто назначается Циклодинон, в состав которого входит прутняк священный.
Очень широкий круг представителей флоры, включаясь в обменные процессы, может позитивно влиять на процесс регулирования гормонального равновесия. Дягиль, корень солодки, пион уклоняющийся, мята и многие другие растения, за которыми далеко ходить не нужно. Готовые сборы продаются в каждой аптеке, а как приготовить лекарство – написано в прилагаемой инструкции.
Диагностика и раннее лечение гиперандрогении (до формирования необратимых клинических проявлений) весьма оправдана с этической точки зрения, ибо запущенный случай, когда девочка уже приобрела мужские черты, от которых невозможно избавиться, очень негативно скажется на ее дальнейшей жизни. Неправильная сексуальная ориентация, необходимость изменения пола, когда человек уже сформирован – большое горе для него самого и его семьи. А ведь при современных методах лечения подобных проблем можно избежать, если не игнорировать предостережения и рекомендации врачей, поэтому такое заболевание, как адреногенитальный синдром ни в коем случае нельзя пускать на самотек.