- Симптомы
- Признаки
- Лечение Операция
- Таргетная терапия
- Химиотерапия
- Иммунотерапия
- 1 стадия
Константин Викторович Пучков Уникальные органосохраняющие операции. Профилактика развития спаечной болезни при помощи современных материалов. Более 500
успешных операций при опухолях почек. Быстрый востановительный период относительно других способов вмешательства
читать полностью
Рак почки – эта болезнь может возникнуть в любом возрасте, однако пик заболеваемости приходится на 50-60 лет. За последние годы количество заболевших увеличилось вдвое. В Европе ежегодно диагностируется около 4 тысяч новых случаев заболевания. Причины болезни до конца не изучены, однако факторы риска сегодня не вызывают сомнений: курение, взаимодействие с химическими веществами, некоторые хронические и наследственные заболевания, ожирение и др.
Что известно о причинах?
Конкретные причины не установлены. Поражение паренхимы почек имеет связь с:
- наследственностью;
- курением;
- гормональными изменениями;
- профессиональными вредностями (контакт с асбестом);
- качеством питьевой воды.
Они рассматриваются в качестве факторов риска.
Больше информации получено о причинах перерождения уротелия (эпителий, покрывающий лоханки). К канцерогенным химическим веществам относятся:
- бензидин, амины, мышьяк;
- переходноклеточный рак лоханок более распространен среди жителей города;
- курение связывают с количеством сигарет и длительностью «стажа», установлено, что в моче курильщиков накапливаются продукты распада триптофана, которые по структуре являются канцерогенами;
- нахождение в лоханках камней вызывает раздражение и разрастание участков эпителия, что способствует возникновению плоскоклеточного рака;
- гипертензия и лечение диуретиками повышает риск рака в 2 раза.
Иммунотерапевтические подходы
Специфическая иммунотерапия характеризуется использованием вакцин, которые изготавливают, используя опухолевые клетки. Вакцины снижают возникновение рецидивов на 10%. При опухоли с метастазами вакцинация малоэффективна. Наиболее эффективной среди вакцин, считается «Онкофаг». Производят препарат из белка теплового шока и опухолевой ткани. «Онкофаг» понижает риск рецидива на 55%. Для вакцин используют:
- девитализированные клетки;
- генетически модифицированные живые клетки;
- пептиды;
- немодифицированные опухолевые, эмбриональные клетки.
По данным разных авторов, резорбция опухолевых очагов после удаления первичного очага при отсутствии какого-либо системного воздействия наиболее характерна для легочных метастазов небольших размеров и отмечается в 0,4-2,5% наблюдений (табл. 2.11).
Таблица 2.11. Спонтанные регрессии после нефрэктомии у больных с отдаленными метастазами
1) неспецифическая иммунотерапия посредством цитокинов (модификаторы биологического ответа);
3) генная терапия на основе Т-лимфоцитов (TIL, натуральные киллеры (NK)) и противоопухолевых вакцин;
4) вакцинотерапия с использованием дендритных клеток (DC) и туморассоциированных антигенов (ТАА);
5) терапия моноклональными антителами.
В настоящее время иммунотерапия цитокинами в клиническом отношении представляется более изученной и является стандартом в лечении диссеминированного рака почки.
Все интерфероны являются гликопротеинами, которые вырабатываются главным образом клетками иммунной системы в ответ на стимуляцию онкогенами, вирусными антигенами, митогенами и др. Впервые они были описаны в 1957 г. A. Isaaks и J.U. Lindenmann как противовирусные, иммуномодуляторные и анти-пролиферативные вещества.
• I класс: интерфероны а — синтезируются макрофагами и лейкоцитами;
• II класс: интерферон в — вырабатывается фибробластами и эпителиальными клетками;
• III класс: интерферон у — секреткруется различными субклассами лимфоцитов (CD4 , CDS , NK, LAK).
• активация натуральных киллеров и цитотоксических Т-лимфоцитов (интерфероны а и в), моноцитов-макрофагов (интерферон у);
• усиление экспрессии антигенов I класса главного комплекса гистосовместимости (ГКГ) — интерфероны а и в, II класса ГКГ — интерферон у;
• антипролиферативная активность в отношении опухолевых клеток (интерфероны а и в);
• ингибирование ангионеогенеза (интерфероны а и в);
• усиление продукции антител В-лимфоцитами (интерферон у);
• индукция рецепторов для интерлейкина-2 (ИЛ-2) (интерферон у);
• взаимодействие с другими факторами и цитокинами (интерфероны а и в). Фармакокинетика интерферона а отличается некоторым своеобразием.
Внутривенное его введение в дозе 10 млн ME приводит к возрастанию уровней сывороточных интерферонов до 1000 Ед/мл, а при введении аналогичной дозы интерферонов у и в — только до 100 Ед/мл. При внутримышечном или подкожном введении интерферона а уровень сывороточных интерферонов повышается до 100 Ед/мл и не изменяется в случае применения интерферонов у и в.
Опыт применения интерферонов у и в при почечно-клеточном раке (ПКР)небольшой, и по эффективности они уступают интерферонам а. Как правило, интерфероны II и III классов не используются в стандартных иммунотерапевтических комбинациях.
Следует отметить, что длительное применение интерферона а вызывает образование против него антител, а это значительно снижает его терапевтический эффект. Причем подтип а2а является более иммуногенным, чем а2в.
Предполагают, что среди всего многообразия свойств интерферона а его терапевтический эффект опосредуется тремя основными механизмами: во-первых, прямое действие на опухолевые клетки путем регуляции процессов клеточной пролиферации и дифференцировки; во-вторых, восстановление и активация дефектных механизмов противоопухолевой защиты и, наконец, ингибирование ангиогенеза в ткани опухоли.
К настоящему моменту уже накоплен достаточный опыт применения интерферона а в качестве монотерапии для лечения больных метастатическим ПКР. Подкожное или внутримышечное введение препарата оказалось предпочтительнее внутривенных инфузий, так как обеспечивало более длительное поддержание терапевтических концентраций препарата в организме больных, а также ассоциировалось с меньшим числом побочных эффектов.
Таблица 2.12. Эффективность интерферона а2 при метастатическом раке почки
Несмотря на различия в результатах иммунотерапии, исследователи пришли к выводу, что большая эффективность интерферона а характерна для больных с удовлетворительным исходным соматическим статусом и отсутствием первичной опухоли. По данным Neidhart и соавт., в случае метастатического изолированного поражения легких частота объективного ответа (количество полных и частичных ремиссий) может достигать 30%.
В настоящее время совершаются попытки усиления действия интерферона а путем комбинированного его использования с различными цитостатическими агентами и ретиноидами. Авторами показана возможность их синергизма в противоопухолевом воздействии, однако отсутствие однозначных выводов на данном этапе диктует необходимость продолжения исследований.
Таким образом, внедрение в клиническую практику интерферона а позволило несколько улучшить результаты лечения больных диссеминированным раком почки. Кроме того, ученым удалось выделить ряд клинических характеристик, влияющих на эффективность иммунотерапии. Действительно, больные с хорошим исходным соматическим статусом, предшествующей нефрэктомией, ограниченным числом метастазов (преимущественно в легких), длительным безрецидивным периодом и коротким интервалом между диагностированием метастазов и началом системного лечения имеют более благоприятный прогноз.
ПОДРОБНОСТИ: Лечение лучами при раке груди
Интерлейкины
Интерлейкины — следующая группа цитокинов, включающая в себя до 22 разновидностей. В онкологической практике наиболее изучен и эффективен ИЛ-2, секреция которого осуществляется Т-лимфоцитами (преимущественно CD4 ) после их активации. Основные свойства ИЛ-2 в формировании противоопухолевого иммунитета сводятся к активации цитотоксических Т-лимфоцитов и усилению их свойств, ускорению роста и дифференцировки специфических В-лимфодитов, стимуляции противоопухолевой активности макрофагов и NK, активации клона льной пролиферации антигенспецифических Т-лимфоцитов, индукции и секреции цитокинов, таких как интерферон у, фактор некроза опухоли,
Впервые ИЛ-2 на большом клиническом материале применил Rosenberg в 1988 г. Из 139 больных, получавших ИЛ-2, 54 страдали метастатическим раком почки. Частота полных и частичных ремиссий в этой группе составила 33%. Больные имели различные локализации метастатических очагов, в том числе легкие, кости, печень, мягкие ткани, лимфатические узлы.
Длительное время считалось, что эффективно только высокодозное болюсное введение ИЛ-2. Использовались 15-минутные инфузии ИЛ-2 в дозе 600 000 МЕ/кг или 720 000 МЕ/кг каждые 8-12 ч в течение 5 дней, с последующим 9-дневным интервалом, за которым следовало повторение цикла. G. Fyfe и соавт. применили описанную методику у 255 больных.
Ремиссии заболевания удалось достичь у 37 больных (15%): в 7 случаях полной и в 20 — частичной. Медиана продолжительности иммунного ответа соответствовала 54 мес (от 7 до 107). Медиана частичных ремиссий составила 20 мес (от 3 до 97). Медиана выживаемости для всей группы больных — 16,3 мес.
Следует отметить, что все больные, включенные в исследование, имели удовлетворительный соматический статус с адекватной дыхательной, сердечной и почечной функцией, множественные метастазы различных локализаций. Однако этот режим терапии сопровождался высокой токсичностью, основными проявлениями которой были фебрильная лихорадка, гипотензия, аритмии, лейкопения, тромбоцитопения и в некоторых случаях почечная недостаточность.
В результате для более половины больных потребовались дополнительные лечебные мероприятия по купированию описанных состояний, включая реанимационные мероприятия, а в 4% наблюдений токсические реакции привели к летальному исходу. Авторы также выделили факторы, влияющие на увеличение частоты объективного ответа: время от диагностирования заболевания и введения ИЛ-2, предшествующая нефрэктомия, изолированное метастатическое поражение легких.
Law и соавт. суммировали результаты 39 клинических исследований, большинство из которых были проведены в рамках II фазы, по применению ИЛ-2 у 1291 больного диссеминированным раком почки. Авторы разделили больных на три группы, ориентируясь на режимы введения ИЛ-2.
В 1-й группе инфузии высоких доз ИЛ-2 осуществлялись внутривенно (в/в) болюсно в стационаре, во 2-й группе больные также наблюдались в условиях клиники, однако инъекции осуществлялись подкожно, к 3-й группе принадлежали больные с амбулаторными режимами введения низких доз препарата (9-18 млн МЕ/сут) подкожно (п/к). Эффективность ИЛ-2 составила 19, 15 и 20% соответственно.
Какие бывают опухоли в почках?
Опухоли почек делятся по происхождению:
- первичные – возникают внутри органа;
- метастатические – заносятся с кровью из разных пораженных тканей.
По локализации на новообразования:
- односторонние (рак правой почки или левой);
- двухсторонние;
- единственной почки.
По отношению к почечным структурам:
- опухоли паренхимы;
- лоханок.
По гистологическому строению на:
- доброкачественные;
- злокачественные (встречаются чаще).
Среди злокачественных новообразований паренхимы наиболее распространены:
- почечно-клеточный рак – наиболее часто выявляется у взрослых людей;
- опухоль Вильмса (еще называется нефробластомой) – болеют преимущественно дети;
- саркома.
В лоханке развиваются:
- переходно-клеточный и плоскоклеточный рак;
- слизистожелезистая опухоль;
- саркома.
По измененному виду клетки врачи-цитологи дают свое заключение
В терминологии онкологов для характеристики степени злокачественности признаков применяется термин «дифференциация опухолевых клеток». Злокачественные клетки возникают из нормальных, постепенно теряют свои функции:
- дифференцированные опухоли можно различить по принадлежности к типу тканей;
- малодифференцированные – сложно отнести к конкретному органу или ткани;
- недифференцированные – отличаются полной потерей функций, клетка может только размножаться, это наиболее опасный тип, отличающийся быстрым прогрессирующим ростом.
В международной классификации принята система TNM. Сочетание буквенно-цифрового обозначения указывает на:
- Т (tumor) – размеры опухоли, прорастание в окружающие ткани, надпочечники, венозную систему;
- N (nodi limphatici) – вовлечение лимфатических узлов;
- М (metastasis) – процесс метастазирования.
Иммуноредактирование
Здоровая иммунная система не позволяет опухоли стать клинически значимой. Способность иммунитета контролировать опухоль — иммуноредактирование — это результат трех процессов, которые происходят одновременно или последовательно:
- элиминация (elimination) — иммунологический надзор, при котором в естественных условиях опухолевые клетки успешно ликвидируются иммунитетом как внешним супрессором;
- равновесие (equilibrium) — иммунный контроль над ростом и размножением трансформированных клеток;
- ускользание (escape) — формирование клеточных вариантов со сниженной иммуногенностью или способностью ослаблять иммунологический ответ.
Идеи об элиминации и ускользании сформированы на основе экспериментальных данных: у иммунодефицитных животных в сравнении с «дикими» чаще развиваются индуцированные и спонтанные опухоли, а опухолевые клетки иммунодефицитных животных более иммуногенны [24].
Оригинал статьи опубликован в газете «Урология сегодня», № 1, 2016 г.
Стадии развития рака почки
Для оптимального выбора лечения необходимо установить стадию развития рака.
Стадия 1 – размеры опухоли до 7 см, расположение внутри почечной капсулы.
Стадия 2 новообразование превышает 7 см, но пока не выходит за пределы почечных границ.
Стадия 3 – имеет 2 варианта:
- опухоль прорастает в крупные вены или в околопочечную клетчатку, не затрагивает надпочечники, лимфатические узлы и фасцию, прикрывающую поверхность почечной капсулы (Герота);
- опухоль любого размера, но не выходит за пределы фасциальных листков, распространяется на ближайшие лимфатические сосуды и узлы.
Последняя стадия 4 – возможна в двух вариантах:
- опухоль заходит за пределы фасции Герота, прорастает в надпочечники, возможно метастазирование в региональные лимфоузлы;
- новообразование имеет любой размер, расположено за границей почек, метастазы имеются как в региональных лимфоузлах, так и в других органах.
Определить стадию можно учитывая размеры опухоли и особенности прорастания
Опухоли могут быть доброкачественными и злокачественными
Доброкачественные опухоли не являются раком и редко бывают опасными для жизни. Как правило, доброкачественные опухоли легко удаляются хирургическим путем и повторно не появляются.
Злокачественная опухоль — более серьезное заболевание, чем доброкачественное новообразование. Злокачественную опухоль можно удалить, но есть риск ее повторного роста. Злокачественные клетки вторгаются и повреждают соседние ткани, а проникнув в лимфатические или кровеносные сосуды, они могут распространиться в другие органы и ткани. Т. е. раковые клетки распространяются из первичного очага с образований новых опухолей в других органах — этот процесс носит название метастазирования.
Опухоли в почечной паренхиме
Далее рассмотрены варианты наиболее распространенных опухолевых процессов.
Почечно-клеточный рак
Почечно-клеточный рак локализуется в корковом веществе, возникает из эпителия канальцев. Относится к самой частой онкологической патологии почек. Хотя наиболее подвержены болезни мужчины после 40 лет, появилась тенденция к «омоложению».
Различий в поражении верхнего и нижнего полюсов почки не выявлено. Рак левой почки развивается по частоте одинаково с правой.
По морфологическому строению представлен шестью типами:
- светлоклеточным или гипернефромой (составляет от 60 до 85%);
- хромофильным или папиллярным (от 7 до 14%);
- хромофобным (от 4 до 10%);
- онкоцитарным (от 2 до 5%);
- клетками собирательных протоков (от 1 до 2%);
- смешанной формой.
Светлоклеточный рак самая распространенная форма, его еще именуют аденокарцинома или гипернефроидный рак почки. Отмечено стимулирующее влияние ожирения, сахарного диабета на развитие опухоли. Клинические проявления чаще незначительные, поэтому пациенты обращаются в запущенной стадии.
По степени дифференцирования опухолевую ткань делят на 5 типов. Они обозначаются буквой G. Чем больше цифра (от G1 до G4), тем менее похожи клетки опухоли на нормальные.
Место, куда метастазирует опухоль, определяется лимфогенным или гематогенным процессом распространения. В первую очередь поражаются ближайшие лимфоузлы, расположенные в зоне ворот, окружающие брюшную аорту и нижнюю полую вену. С кровью метастазы заносятся в органы, обильно снабженные сосудами.
По частоте отдаленных метастазов при раке почки они распределяются так:
- в легкие;
- в костную ткань;
- в клетки печени;
- в головной мозг.
Метастазы, могут появиться спустя несколько лет после удаления почки с первичной опухолью.
Ангиомиолипома почки — опасна ли она для жизни
Клинические проявления включают:
- макрогематурию (видимые примеси крови в моче);
- боли в области поясницы, возможно, в виде почечной колики, интенсивность зависит от стадии процесса;
- варикоцеле у мужчин (увеличение яичка);
- пальпируемое плотное образование в области нижнего полюса почки;
- умеренное повышение температуры тела на длительный период, редко она доходит до высоких цифр, пациента знобит;
- головные боли на фоне гипертензии;
- отсутствие аппетита;
- слабость;
- потерю веса.
Подробнее узнать о клинических проявлениях рака почки и особенностях его диагностики можно в этой статье.
Дифференциальную диагностику почечно-клеточного рака следует проводить с:
- Кистой почки – образование можно пропальпировать, оно на ощупь мягкое и эластичное, на УЗИ и компьютерной томограмме выглядит как тело со сниженной эхогенностью, но с четкими контурами. Онкологи учитывают способность рака развиваться внутри кисты. Поэтому при любых вмешательствах рекомендуется цитологическое исследование содержимого.
- Гидронефрозом – пальпируется нетвердое образование, УЗИ и экскреторная урограмма дают окончательную картину.
- Поликистозом – при пальпации определяются жесткие бугры, в диагностике помогают аппаратные способы.
- Абсцессом почки – даже при проведении УЗИ и экскреторной урографии может ошибочно расцениваться как опухоль, помогают компьютерная томография, ангиографическое исследование сосудов.
Онколог — врач, который помогает больным в борьбе с раком
Похожая рентгенологическая и УЗИ-картина новообразования возникает при:
- лимфогранулематозе;
- неходжкинских лимфомах;
- формировании артериовенозных свищей;
- метастазах в почки рака других органов.
Особенности нефробластомы
Нефробластома или опухоль Вильмса развивается у детей в возрасте от 2 до 5 лет. Реже в других группах. У взрослых – очень редкие случаи. Одинаково часто встречаются у девочек и мальчиков. Только в 5% случаев нефробластома поражает обе почки.
Считается, что причиной являются нарушения эмбрионального развития. Среди генетических мутаций главная роль принадлежит группе генов, которые создают в почечной паренхиме предрасполагающие участки ткани. Они после рождения ребенка могут превратиться в нормальные клетки или остаются и позже перерождаются в злокачественные.
Опухоль сопутствует врожденным аномалиям мочеполовых органов:
- сращению почек;
- крипторхизму.
Иногда у ребенка одновременно наблюдается отсутствие радужной оболочки глаз.
Клинические проявления такие же, как при почечно-клеточном раке у взрослых. Гематурия встречается у каждого десятого пациента. Боли считаются нехарактерными. Возникают только при значительном разрастании опухоли в брюшину, печень, диафрагму.
Опухоль у малыша безболезненна, пальпируется легко
Малыш хорошо себя чувствует. При осмотре обнаруживают крупную гладкую опухоль в животе. Бугристость встречается редко. Метастазирование не отличается от рака почек у взрослых. Увеличена вероятность тромбообразования на уровне почечной и нижней полой вен.
Симптомы заболевания
На ранней стадии болезнь протекает бессимптомно. Лишь у 20% пациентов отмечается классическая триада: гематурия, боль в животе или пояснице, прощупывание объемного образования. Но чаще наблюдается не триада, а один или два признака, причем не всегда пациент уделяет должное внимание появившимся симптомам. Так, гематурия может начаться внезапно, быть безболезненной, кратковременной и прекратиться самостоятельно. Боль в поясничной области наблюдается у 60-70% пациентов. Больного беспокоит дискомфорт, чувство тяжести, иногда типичная почечная колика. Прощупать злокачественное образование обычно удается, когда опухоль достигла больших размеров. Однако, появление этих симптомов свидетельствует о том, что заболевание перешло на более позднюю стадию.
У 25% пациентов к моменту установления диагноза имеются отдаленные метастазы и клиническая картина обусловлена метастазированием. При поражении легких отмечаются кашель, одышка и кровохарканье, при распространении метастазов в кости наблюдаются боли, патологические переломы, поражение печени характеризуется желтухой, повышением температуры, увеличением печени, болезненностью в правом подреберье. У 15% больных возникает гипертензия, трудно поддающаяся коррекции. При злокачественном образовании в почке характерно расширение вен передней брюшной стенки, варикоцеле, отеки нижних конечностей и др.
Раковые опухоли в почечной лоханке
Локализация рака в области лоханок встречается в 7-10% всех случаев опухолей почек. первичные опухоли происходят из уротелия. По гистологии злокачественные эпителиальные новообразования делятся в зависимости от типа клеток на:
- переходно-клеточный рак – встречается у почти 99% пациентов;
- плоскоклеточный рак – частота выявления от 1 до 8%;
- аденокарциному – очень редкая форма.
Важной особенностью является возможность образования сразу нескольких очагов озлокачествления (малигнизации). По этому признаку рак лоханки делится на:
- единичное новообразование;
- множественное (у 20% больных).
Кроме того, следует учитывать возможность поражения одной или обеих почек. Выявить все очаги важно для лечения.
В классификации лоханочного поражения выделяют опухоли:
- локализованные – находятся в пределах лоханки;
- регионарные – прорастают в другие почечные структуры, околопочечные ткани и органы, лимфатические узлы;
- метастатические – распространяются в отдаленные органы.
Примером множественных злокачественных очагов в лоханке является папиллярный рак почки (до 16% от всех опухолей лоханки). Он образуется из переходного эпителия. Эта форма особенно распространена на Балканах (25%).
Особенность метастазов – распространение с мочой на мочеточники и мочевой пузырь. Канцерогенные вещества, накопившиеся в крови, сначала вызывают формирование папиллом. Впоследствии они перерождаются в папиллярный рак почки.
Более агрессивными свойствами обладают метастатические очаги. Рост начинается с уротелия, может здесь остановиться или проникнуть вглубь мышцы.
Видимое окрашивание мочи указывает на макрогематурию
Среди симптомов рака лоханок главными служат:
- гематурия – наблюдается у 95% пациентов, из-за нее больные приходят к врачу;
- боли в пояснице – имеются у половины больных.
Такие общие симптомы, как похудание, потеря аппетита, небольшая температура возникают реже. Дизурическая симптоматика выявляется у 10% больных.
Какие осложнения возможны при откладывании обследования и лечения
Для данного заболевания характерна тройка клинических признаков, но присутствие всех симптомов триады совсем не обязательно:
- Кровь в моче от выявления при анализе эритроцитов и до «кровавой» мочи.
- На уровне пупка в животе прощупывается опухоль.
- Не связанная с движениями и нагрузкой боль в пояснице или подреберье.
Не относятся к типичным признакам, но часто встречаются в разных сочетаниях:
- Повышение артериального давления, которое пациент абсолютно не чувствует.
- Стойкое и «беспричинное» — при отсутствии каких-либо признаков воспаления повышение температуры.
- Варикоцеле — увеличение сосудистого рисунка и расширение поверхностных вен яичка.
- Снижение уровня эритроцитов и гемоглобина в крови — анемия.
- Сгущение крови с существенным повышением уровня эритроцитов — полицитемия.
- Снижение веса без уменьшения объёма потребляемой пищи.
- Рассеянные боли в мышцах и их слабость.
Средняя выживаемость при своевременном корректном лечении онкологии почки I и II стадии:
- Пятилетняя выживаемость — 95%.
- Средняя продолжительность жизни — 15 лет.
Средняя выживаемость при ошибочном и запоздалом лечении онкологии почки III и IV стадии:
- Пятилетняя выживаемость — 5%.
- Средняя продолжительность жизни — 1,5 года.
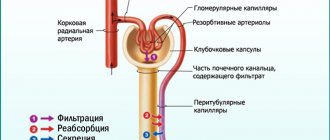
Можно ли диагностировать опухоль на УЗИ?
Воздействие ультразвука на ткани организма похоже на возврат эха. Поэтому картину на мониторе называют эхограммой. Метод позволяет диагностировать опухоль по плотности ткани. К сожалению, он дает только общую информацию о локализации, размерах, выходе за пределы капсулы. Но в дифференциальной диагностике не помогает.
Если плотность опухолевых клеток мало отличается от нормальных, то новообразование считается эхонегативным, методом УЗИ его выявить невозможно. В практике применяют для контроля за пункционной биопсией, направлением иглы.
Картина опухоли левой почки лучше всего видна на компьютерной томограмме в разных проекциях
Когда показана лапароскопическая резекция?
У пациентов с опухолью на стадиях Т1 и Т2 (локализованная опухоль, не выходящая за пределы органом) хирургическое вмешательство является эффективным методом лечения, обеспечивающим пятилетнюю выживаемость около 95%.
Раньше резекция при раке была показана лишь пациентам с единственной почкой, плохой функцией обеих почек или с двусторонним поражением злокачественным процессом. Всем остальным пациентам выполнялась радикальная нефрэктомия. Однако с 1990-ых годов показания к выполнению данного вмешательства расширились и операция частичной нефрэктомии была одобрена для лечения пациентов с небольшими опухолями (Т1 иТ2).
Таким образом, лапароскопическая резекция представляет собой органосохраняющее оперативное вмешательство, одобренную для пациентов с опухолью не более 4 см в диаметре. Хотя нередко к данной операции прибегают и при больших размерах опухоли.
На сегодняшний день подавляющее большинство исследований показали эквивалентную эффективность борьбы у пациентов, которым выполнялась радикальная нефрэктомия или резекция почки.
Своевременное лечение рака должно быть радикальным. Узнайте подробности
Проблемы лечения рака почки
Лечить рак почки необходимо в ранней стадии, когда опухолевые клетки располагаются поверхностно, не врастают во внутрь органа и не дают метастазов. Метод лечения выбирается после полного обследования.
К нехирургическим способам относятся:
- криодеструкция – замораживание растущих клеток жидким азотом;
- радиочастотная абляция – использование радиоволн высокой частоты только при небольших опухолях, не связанных с сосудами;
- таргетная терапия при раке почки – назначение медикаментов прицельного действия на перерожденные ткани;
- лучевое воздействие на опухолевые клетки.
Иммунотерапия при раке почки проводится с целью активизации борьбы организма со злокачественными образованиями. Применяются α-Интерферон изолированно или в комбинации с Интерлейкином. Эффект появляется у 1/5 пациентов в виде более или менее длительной ремиссии.
Химиотерапия при раке почки потеряла свое значение. Это вызвано низкой чувствительностью почечно-клеточного рака к цитостатикам. Опухоль выделяет биологически активные вещества, снижающие воздействие лекарств. Продолжают назначать Винбластин, 5-флуороурацил в комбинации с иммунотерапией.
Лучевая терапия также малоэффективна. Не все онкологи назначают ее. Не вызывает сомнений использование метода в терапии рака почки с метастазами в головной мозг, легкие, кости.
Ученые ведут разработки ожидаемых с большой надеждой иммунопрепаратов на основе молекулярной генетики и специфических вакцин.
В лечении локализованных опухолей применяется хирургический способ. Наиболее распространена операция радикальной нефрэктомии. Удаление почки при раке проводят вместе с окружающей жировой клетчаткой, региональными лимфоузлами (диафрагмальными, бифуркационными).
Если опухоль проросла в венозную систему приходится удалять часть сосудов. Такая же участь приготовлена для надпочечников при прорастании опухоли в верхний полюс. Органосохраняющей операцией называют частичную резекцию почки с удалением опухолей небольших размеров (до 4 см). Она показана:
- при раке единственной почки;
- двухстороннем поражении почки;
- при полностью нарушенной функции второй почки.
В последние годы получили распространение оперативные техники с применением лапароскопа. Эти операции с хорошим результатом входят в лечение рака почки в Израиле.
Пациентам в запущенной стадии с метастазами удалить почку невозможно. Применяются терапевтические методы воздействия. Общая доля таких больных доходит до 30%.
Редко удаляют почку вместе с метастазами. На это идут при выраженном болевом синдроме, постоянной кровопотере. После удаления удается терапевтическими методами скоррегировать анемию, снять боли.
При лечении опухоли Вильмса у детей используют хирургические методы в комбинации с химио- и лучевой терапией. Учитываются размер и дифференциация опухоли, возраст ребенка.
При одностороннем процессе удаление почки производят через брюшинный доступ, в случае двухстороннего поражения – не удаляются, а частично резецируются обе почки.
Эту операцию проводят даже при наличии отдаленных метастазов.
Важно, что опухоль Вильмса чувствительна к лучевому воздействию. Но радиоактивное излучение нарушает развитие ребенка. Поэтому используется ограниченно только в послеоперационном периоде в случаях прогностически неблагоприятно протекающих опухолей. До операции при этом виде рака почки таргетная терапия наиболее показана.
Для химиотерапии детей используют цитостатики:
- Винкристин;
- Дактиномицин;
- Доксорубицин;
Дозировки назначаются по весу и возрасту ребенка.
Для уменьшения токсического действия препаратов используют пульс-терапию – короткие курсы больших доз. Лечение рака почки народными средствами категорически запрещено. Под воздействием применяемых препаратов значительно снижается защитная реакция организма. Отвары трав могут вызвать нежелательную реакцию.
Хирургическое лечение — один из методов радикальной борьбы с опухолью
Литература
- Rosenberg S.A., Lotze M.T., Muul L.M., Leitman S., Chang A.E., Ettinghausen S.E. et al. (1985). Observations on the systemic administration of autologous lymphokine-activated killer cells and recombinant interleukin-2 to patients with metastatic cancer. N. Engl. J. Med. 313, 1485–1492;
- Fisher R.I., Rosenberg S.A., Fyfe G. (2000). Long-term survival update for high-dose recombinant interleukin-2 in patients with renal cell carcinoma. Cancer J. Sci. Am. 6 (Suppl 1), S55–S57;
- Демидов Л.В., Харкевич Г.Ю., Тимофеев И.В. (2003). Успехи и неудачи применения цитокинов в лекарственной терапии некоторых солидных опухолей. Практическая онкология. 4, 140–147;
- Cao Y. and Langer R. (2008). A review of Judah Folkman’s remarkable achievements in biomedicine. Proc. Natl. Acad. Sci. USA. 105, 13203–13205;
- Lainakis G. and Bamias A. (2008). Targeting angiogenesis in renal cell carcinoma. Curr. Cancer Drug Targets. 8, 349–358;
- Motzer R.J., Escudier B., Oudard S., Hutson T.E., Porta C., Bracarda S. et al. (2008). Efficacy of everolimus in advanced renal cell carcinoma: a double-blind, randomised, placebo-controlled phase III trial. Lancet. 372, 449–456;
- Escudier B., Porta C., Schmidinger M., Rioux-Leclercq N., Bex A., Khoo V. et al. (2016). Renal cell carcinoma: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann. Oncol. 27 (suppl 5), v58–v68;
- Хороший, плохой, злой, или Как разозлить лимфоциты и уничтожить опухоль;
- Иммуностимулирующие вакцины;
- Т-клетки — марионетки, или как перепрограммировать Т-лимфоциты, чтобы вылечить рак;
- Лечение Джимми Картера;
- Folkman J. and Kalluri R. (2004). Concept cancer without disease. Nature. 427, 787;
- Соколов Е.А. (2015). Донорская почка с малыми опухолями: допустима ли трансплантация? Урология сегодня. 4, 12–13;
- Starnes C.O. (1992). Coley’s toxins in perspective. Nature. 357, 11–12;
- FDA approves Opdivo to treat advanced form of kidney cancer. (2015). U.S. Food and Drug Administration;
- Motzer R.J., Sharma P., McDermott D.F., George S., Hammers H.J., Srinivas S. et al. (2016). CheckMate 025 phase III trial: Outcomes by key baseline factors and prior therapy for nivolumab (NIVO) versus everolimus (EVE) in advanced renal cell carcinoma (RCC). J. Clin. Oncol. 34 (suppl 2S), abstr. 498;
- A closer look at CheckMate 025 supports nivolumab benefits across patient subgroups and use as second-line therapy. (2016). The Genitourinary Cancers Symposium;
- Freeman G.J. (2008). Structures of PD-1 with its ligands: sideways and dancing cheek to cheek. Proc. Natl. Acad. Sci. USA. 105, 10275–10276;
- Latchman Y., Wood C.R., Chernova T., Chaudhary D., Borde M., Chernova I. et al. (2001). PD-L2 is a second ligand for PD-1 and inhibits T cell activation. Nat. Immunol. 2, 261–268;
- Watch the video: dr. Gordon Freeman, renal cancer keynote address. (2016). The Genitourinary Cancers Symposium;
- Sheridan C. (2014). First PD-1 inhibitor breezes across finish line. Nat. Biotechnol. 32, 847–848;
- de Velasco G., Krajewski K.M., Albiges L., Awad M.M., Bellmunt J., Hodi F.S., Choueiri T.K. (2016). Radiologic heterogeneity in responses to anti-PD-1/PD-L1 therapy in metastatic renal cell carcinoma. Cancer Immunol. Res. 4, 12–17;
- Meng X., Huang Z., Teng F., Xing L., Yu J. (2015). Predictive biomarkers in PD-1/PD-L1 checkpoint blockade immunotherapy. Cancer Treat. Rev. 41, 868–876;
- Koebel C.M., Vermi W., Swann J.B., Zerafa N., Rodig S.J., Old L.J. et al. (2007). Adaptive immunity maintains occult cancer in an equilibrium state. Nature. 450, 903–907;
- Coley WB. (1891). II. Contribution to the knowledge of sarcoma. Ann. Surg. 14, 199–220.
Как питаться больному при раке почки?
Питание при раке почки должно помочь в работе оставшемуся после операции органу, но не вызывать его раздражения. Поэтому диета при раке почки строится с учетом сбалансирования по энергетическим затратам и потребностям в белке.
Не рекомендуются диетологами:
- соленья и маринады, консервы;
- копченые изделия из мяса и рыбы;
- наваристые бульоны;
- блюда из грибов;
- продукты с солью (сыр, колбасы, сосиски);
- жирные мясные и рыбные блюда, сало;
- бобовые;
- кондитерские изделия и выпечка с кремом;
- газированные напитки;
- любой алкоголь, крепкий чай и кофе.
Можно употреблять:
- отварное или запеченное мясо, супы;
- молочные продукты (творог, кефир, сметану);
- крупяные изделия;
- овощи и фрукты в достаточном объеме.
Для питья рекомендуется варить компот из сухофруктов, готовить отвар шиповника. По поводу употребления соли и общего объема жидкости следует проконсультироваться со своим врачом.
В молодом возрасте выживаемость ниже
Госпитализация
Госпитализация, как правило, осуществляется за один день до операции, т. е. ночь вы проведете в больнице. Иногда госпитализация допустима в день операции, на усмотрение врача. С собой нужно взять туалетные принадлежности, предметы личной гигиены, возможно индивидуально подобранные препарата которые вы принимаете постоянно. В среднем время пребывания в стационаре составляет 5–7 суток.
Материал подготовлен заместителем главного врача по лечебной работе клиники «Медицина 24/7», кандидатом медицинских наук Сергеевым Петром Сергеевичем.
Источники:
- Франк М. А., Санжаров А. Е., Шамуратов Ш. Ш., Усс А. Г., Капустин К. И., Паньшин С. В., Сорочкин Д. А. Лапароскопические операции в лечении рака почки // Медицинский вестник Башкортостана. 2013. №2.
- Шаплыгин Леонид Васильевич, Олефир Юрий Витальевич, Козлов Сергей Васильевич, Горбачев Андрей Львович, Евсеев Дмитрий Сергеевич Хирургическое лечение местно-распространенного рака почки // Медицинский альманах. 2012. №4.
- Лоран О. Б., Серегин А. В., Шустицкий Н. А. Технические особенности при выполнении органосохраняющих операций по поводу рака почки // Медицинский вестник Башкортостана. 2013. №2.
- Чиссов, В.И., Старинский, В.В., Петрова, Г.В. Злокачественные новообразования в России в 2008 году. — М.: ФГБУ «МНИОИ им. П.А. Герцена» Минздравсоцразвития России, 2010. — 196 с.
Что ожидает больного?
Прогноз при раке почки зависит от формы опухоли и стадии начала лечения:
- При раннем выявлении и полноценном лечении в первой стадии рака паренхимы возможно излечение до 90% пациентов.
- Если больной выявлен во второй стадии, длительную ремиссию ожидают у половины перенесших операцию. Отрицательно сказывается потеря до лечения более 10% массы тела.
- При адекватной терапии и наличии метастазов 5 лет живут не более 15% пациентов.
- При переходно-клеточном раке лоханки успешной лечение наблюдается у 90% пациентов.
- Если опухоль проросла вовнутрь, то удовлетворительного результата удается добиться у 15% пациентов.
- При распространении на окружающие органы и наличии метастазов положительного лечения получить пока невозможно.
- Раннее удаление опухоли Вильмса у 90% детей приводит к благополучным последствиям.
На прогноз влияет степень дифференциации злокачественных клеток. Любая симптоматика, похожая на перечисленные признаки, требует скорейшего обращения к врачу.
Отзывы наших пациентов
- Рак почки 4 стадии: Отзыв о лечении
Рак почки 4 стадии: Отзыв о лечении 24 июня 2020 г.Пациенту 61 год. Проходил обследование и лечение в больнице им. С. П. Боткина. Были трудности с постановкой диагноза. После начала эпидемии COVID-19 госпитализация туда стала невозможной. Пациент обратился в клинику «Медицина 24/7». Здесь ему проведено обследование. Поставлен точный диагноз — рак почки 4 стадии с метастатическим поражением костей, легких и головного мозга. Начато полноценное лечение. На момент поступления в области…
читать дальше
- Отзыв о лечении метастатического поражения костей черепа
Отзыв о лечении метастатического поражения костей черепа 7 мая 2018 г.
Владимир Александрович попал в клинику «Медицина 24/7» после многократных отказов в клиниках Нижнего Новгорода и Новосибирска. Опухоль, являющаяся метастазом рака почки, поразила кости черепа в районе теменной области, мягких тканей головы была прооперирована нейрохирургом Игорем Юрьевичем Малаховым. Пациент чувствует себя хорошо, прогноз жизни благоприятный.
читать дальше
Какие осложнения развиваются при откладывании радикального лечения почечно-клеточного злокачественного образования?
- Скорость течения злокачественного процесса индивидуальна, но рост ракового конгломерата неизбежно затронет нижнюю полую вену, сдавление крупнейшего сосуда приведёт к отеку брюшной стенки, на которой появится венозная сеть в виде «головы медузы», а в животе будет накапливаться жидкость — асцит.
- Прорастание опухоли в полую вену сопровождается образованием тромба, отрыв его чреват смертью от тромбоэмболии лёгочных сосудов или инсульта.
- Почка синтезирует гормон эритропоэтин, его недостаточная продукция из-за разрушения органа приводит к глубокой и безнадёжной анемии, при которой непереносимо хирургическое вмешательство, потому что даже небольшую кровопотерю не удастся заместить переливаниями, а химиотерапия невозможна — «убивает» клетки крови.
- Рост опухолевого конгломерата сопровождается распадом тканей в центральной части узла, токсичные продукты всасываются в кровь, вызывая тяжёлую интоксикацию с температурой и истощением — кахексией.
Прогрессирование онкологического заболевания может протекать очень медленно и довольно быстро, но никакие диагностические методики не способны предсказать его реальную скорость, откладывая оперативное вмешательство на пару недель, можно навсегда лишить себя возможности вылечиться.