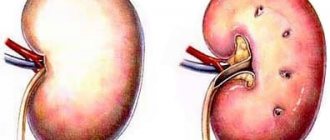
Острая надпочечниковая недостаточность, которая так же называется гипоадреналовым или аддисоническим кризом – это ургентное жизнеугрожающее состояние, при котором значительно снижается или совсем прекращается выработка надпочечниками необходимых организму гормонов, вследствие чего нарушаются его важные функции. Смертность при этом состоянии очень высока: летальный исход происходит более чем в 50 % случаев. Именно поэтому каждому практикующему врачу так необходимо знать о тактике неотложной терапии при возникновении недостаточности надпочечников.
Причины хронической надпочечниковой недостаточности у детей и взрослых
Снижение функции надпочечных желез проявляется при разрушении практически всего коркового слоя, вырабатывающего гормоны. Только в 2% случаев у больных в крови отсутствуют антитела к собственным клеткам. А у остальных по неизученным причинам начинается образование иммуноглобулинов клетками иммунной системы. Они так реагируют на фермент, который принимает участие в образовании кортизола и альдостерона.
Образованные комплексы фермент-антитело откладываются в функционирующей ткани, приводя к ее поражению. Нередко также страдают и другие внутренние органы, чаще всего недостаточность надпочечников сочетается с аутоиммунным тиреоидитом. К числу менее распространенных причин относятся:
- туберкулезная, сифилитическая, ВИЧ-инфекция;
- генетический дефект – не образуется фермент, перерабатывающий жирные кислоты, они скапливаются в нейронах и клетках коркового слоя, нарушая функцию надпочечников;
- изменения свертывающей активность крови;
- метастазы опухолей легких, молочных желез;
- оперативное удаление (адреналэктомия);
- длительные воспалительные процессы в организме, множественные очаги нагноения, сепсис;
- врожденные и приобретенные пороки сердца;
- инфаркт, амилоидоз ткани надпочечников;
- применение кетоконазола (Низорал и аналоги), Верошпирона, некоторых снотворных и антикоагулянтов.
Кроме поражения самих надпочечников, их работа может нарушиться при разрушении органов, регулирующий продукцию кортизола. К таким заболеваниям относятся:
- аденома гипофиза;
- новообразования гипоталамуса;
- геморрагический инсульт гипоталамической, гипофизарной области мозга, инфекционный, аутоиммунный процесс в этой зоне;
- аневризма артерии мозга;
- лучевая терапия тканей головного мозга, операции;
- длительное применение препаратов из группы глюкокортикоидов, подавляющих образование регуляторных гормонов гипофиза и гипоталамуса по принципу обратной связи.
Рекомендуем прочитать статью о болезнях надпочечников. Из нее вы узнаете о том, какие могут быть болезни надпочечников, их гиперфункция и гипофункция, причинах болезней надпочечников, а также о симптомах у детей, женщин и мужчин.
А здесь подробнее о болезни и синдроме Иценко-Кушинга.
Врачебная помощь
В условиях медицинского стационара назначается интенсивная терапия, которая преследует несколько лечебных целей:
Контроль эффективности проводимой терапии выполняется при помощи лабораторных исследований, включая анализы крови, мочи, определение уровня гормонов. Параллельно обязательно выясняются причины патологического состояния и проводится терапевтическое устранение их воздействия.
Прогноз при острой надпочечниковой недостаточности у ребенка зависит от своевременности начала, а также адекватности проводимой терапии. При правильном лечении в течение небольшого промежутка времени функциональное состояние всех систем организма ребенка восстанавливается.
Часто возникает при различных стрессовых ситуациях с латентно существовавшей до этого гипофункцией надпочечников — острая надпочечниковая недостаточность у детей. В этой статье мы рассмотрим основные причины и симптомы острой надпочечниковой недостаточности у детей, а также о том, как проводится лечение острой надпочечниковой недостаточности у ребенка.
Механизм развития
Обменные нарушения при недостаточности надпочечников связаны со снижением образования альдостерона и кортизола клетками коркового слоя. Это приводит к таким изменениям:
- выводится жидкость из организма из-за потерь натрия;
- задерживаются соли калия;
- водно-электролитный дисбаланс препятствует нормальному функционированию почек, кишечника, сердца, сосудов;
- не образуются в достаточном количестве запасы гликогена, что объясняет снижение концентрации глюкозы в крови;
- гипофиз в ответ на нехватку кортизола усиленно продуцирует адренокортикотропный (АКТГ) и гормон, вызывающий потемнение кожи и слизистых (меланоцитостимулирующий).
Проявления недостаточности надпочечников нарастают при воздействии стресса, травматического поражения тканей, операций, инфекционных процессов, обострении сопутствующих болезней.
Классификация патологии
В зависимости от пораженного органа хронически низкая функция надпочечников делится на первичную и центральную, или вторичную и третичную
Первичная
Преобладает среди всех случаев болезни. Ее обнаруживает у 94% пациентов. Развивается при разрушении тканей самих надпочечных желез, симптомы возникают при обширном двустороннем поражении. Среди заболевших преобладают лица зрелого возраста, мужчин и женщин среди них примерно поровну. Другое название этой патологии – аддисонова (бронзовая) болезнь, гипокортицизм.
Вторичная
Возникает при нарушении функции гипофиза, а именно – снижении образования ним адренокортикотропного гормона. При помощи него происходит стимуляция синтеза кортизола корой надпочечников. Поэтому при вторичном гипокортицизме страдают только обменные процессы с его участием, а водно-солевой обмен и альдостерон остаются в норме. Такое течение болезни более благоприятное, чем при первичном нарушении.
К центральным формам болезни, помимо вторичной, относится и третичная недостаточность. Ее вызывает дефицит кортиколиберина, который синтезирует гипоталамус. В его ведении находится образование АКТГ клетками гипофиза. Вне зависимости от места поражения все формы патологии приводят к атрофии коры надпочечников.
Нарушение функций гипофиза
Симптомы хронической надпочечниковой недостаточности
Основной признак, по которому эндокринолог может заподозрить низкую функцию надпочечных желез – это изменение цвета кожи и слизистых. Это нарушение имеет такие характеристики:
- вначале темнеют части тела, на которые чаще всего попадает свет солнца – кожа лица, рук, верхняя часть тела, ноги у женщин, а также зоны, уже имеющие пигментацию – окружность сосков, промежность, область подмышек, кожных складок;
- потемнение затрагивает зоны, подвергающиеся трению одеждой;
- цвет изменяется от оттенка загара до бронзового, затем серого;
- внутренние поверхности ротовой полости, половых органов и кишечника становятся иссиня-черными;
- на фоне темного цвета бывают белые крупные и мелкие пятна – витилиго (только при аутоиммунном происхождении болезни);
- редко бывает белый вариант аддисоновой болезни – кожа бледная, плохо загорает на солнце (обычно встречается при вторичной недостаточности).
Пациентка до и после лечения надпочечниковой недостаточности
Второе типичное изменение – похудание. Оно может быть незначительным (до 5 кг) или доходить до истощения (15-30 кг). Больные склонны к депрессии, потере интереса к окружающему, снижению полового влечения. Их беспокоит постоянная слабость, даже обычная активности дается с трудом, утрачивается работоспособность.
При резкой смене положения тела появляется головокружение, потемнение в глазах, а в стрессовой ситуации они теряют сознание. Практически все пациенты гипотоники, нормальное давление встречается только при исходной (до аддисонизма) гипертонической болезни.
У большинства нарушается переваривание и усвоение пищи – низкий аппетит, боль в подложечной области, неустойчивый стул с чередованием поносов и запоров, тошнота и рвота, вынуждающие отказываться от еды. Из-за существенных потерь натрия при дефиците альдостерона появляется пристрастие к соленой пище, может быть непреодолимое желание есть соль даже без продуктов, в чистом виде.
Для вторичной недостаточности гиперпигментация, низкое давление и влечение к соли не характерны, так как уровень альдостерона не меняется. Из-за понижения содержания кортизола больные жалуются на общую слабость, которая усиливается через 2-2,5 часа после еды. Последний симптом связан с тем, что падает концентрация глюкозы в крови при выделении инсулина, а запаса ее виде гликогена нет.
Неотложные мероприятия
Острая надпочечниковая недостаточность — абсолютное показание к госпитализации. Лечение проводят в специализированном ОРИТ. В начале лечения, особенно если пациент находится в бессознательном состоянии, необходимо установить мочевой катетер и желудочный зонд.
Регидратация
Не дожидаясь результатов гормональных исследований, как можно раньше начинают внутривенное введение 2–3 л 0,9% раствора натрия хлорида. Скорость инфузии должна составлять 500 мл/ч (при коллаптоидном состоянии — струйно). В дальнейшем к изотоническому раствору натрия хлорида добавляют 5–10% раствор глюкозы. За первые сутки вводят не менее 4 л жидкости. Введение калийсодержащих, гипотонических растворов и диуретиков противопоказано.
При многократной рвоте рекомендуют внутривенное введение 10–20 мл 10% раствора хлорида натрия в начале лечения и повторное введение при выраженной гипотонии. Кроме изотонического раствора хлорида натрия и глюкозы, при необходимости назначают полиглюкин в дозе 400 мл, плазму крови.
Заместительная глюкокортикоидная терапия
Препарат выбора — гидрокортизон. В больших дозах он обеспечивает как глюко-, так и минералокортикоидный эффект.
Гидрокортизона гемисукцинат (солу-кортеф) вводят как внутривенно, так и внутримышечно. Суспензию гидрокортизона ацетата необходимо вводить только внутримышечно. Гидрокортизонаацетат действует несколько более длительно, чем гемисукцинат.
Одномоментно гидрокортизон вводят внутривенно струйно в дозе 100 мг. Далее в течение первых суток вводят 100 мг препарата внутривенно или внутримышечно каждые 6–8 ч. В течение первых суток общая доза гидрокортизона составляет 400–600 мг, реже (в тяжелых случаях) — 800–1000 мг, иногда и больше.
При отсутствии гидрокортизона возможно внутривенное введение 4–8 мг дексаметазона с последующим переходом на терапию гидрокортизоном.
Внутривенное введение гидрокортизона продолжают до выведения больного из коллапса и повышения систолического АД более 100 мм рт.ст. На 2-е–3-и сутки, когда состояние больного стабилизируется, дозу гидрокортизона постепенно снижают до 150–200 мг/сут, далее продолжают его внутримышечное введение 4–6 раз в сутки в дозе 50–75 мг.
Когда доза гидрокортизона станет менее 100 мг/сут, к терапии добавляют флудрокортизон (кортинефф) в дозе 0,1 мг/сут. При суточной дозе гидрокортизона более 100 мг нет необходимости в назначении минералокортикоидов.
Обычно для достижения поддерживающей дозы гидрокортизона необходимо до пяти дней. Лечение гормональными препаратами нужно проводить в адекватных количествах под контролем содержания натрия, калия и сахара в крови, а также АД. Недостаточная эффективность лечения аддисонического криза может быть связана с малой дозой гормональных препаратов или растворов солей, быстрым снижением дозировки препаратов.
Антибиотикотерапия
При лихорадке (за исключением возникшей на фоне выраженной дегидратации) антибиотики следует назначать даже при отсутствии явного очага инфекции.
Симптоматическая терапия
При невозможности стабилизировать гемодинамику одними глюкокортикоидами показано дополнительное введение катехоламинов и аналептиков.
Дальнейшее ведение
После стабилизации состояния пациента и снижения суточной дозы гидрокортизона менее 100 мг/сут пациента переводят на постоянную заместительную терапию таблетированными препаратами гидрокортизона.
Осложнения
Если пациент не обращается к эндокринологу или не выполняет его рекомендации, лечится самостоятельно с применением нетрадиционных методов, то возникает аддисонический криз. При нем появляются такие опасные симптомы:
- утрата сознания – оглушенность, прострация;
- падение давления крови, коллапс или шок;
- обильная рвота и понос, быстрая дегидратация (обезвоживание);
- накопление кетоновых тел в крови, запах ацетона в выдыхаемом воздухе;
- судорожные припадки;
- декомпенсация сердечной деятельности.
Это осложнение может иметь три варианта течения, расстройства преимущественно затрагивают:
- нервную систему – головная боль, судороги, несвязная речь, заторможенность, нарушения сознания различной степени выраженности;
- сердце и сосуды – падение давления, бледная и холодная кожа, посинение кончиков пальцев, носогубного треугольника, учащенное сердцебиение, слабый пульс, обморочное состояние, прекращение выделения мочи;
- пищеварительную систему – спазмы, колики в животе, тошнота с неукротимой рвотой, вздутие живота, понос со слизью или прожилками крови.
Такая симптоматика с трудом поддается лечению, поэтому развитие криза рассматривается как угроза для жизни пациента.
Смотрите на видео о хронической недостаточности надпочечников:
Клинические проявления
Симптоматика развития острого ургентного состояния зависит от возраста ребенка. Надпочечниковая недостаточность у детей в возрасте до полугода характеризуется появлением таких признаков:
При отсутствии адекватной неотложной помощи и выполнения терапевтических мероприятий признаки нарастают, критически снижается артериальное давление и развивается коллапс. У детей более старшего возраста на начальных стадиях развития патологического процесса беспокоят головные боли и выраженные ощущения дискомфорта в животе. Затем по мере прогрессирования недостаточности функциональной активности надпочечников присоединяется выраженное снижение уровня системного артериального давления, уменьшение мочеиспускания (олигурия) вплоть до его полного отсутствия (анурия). Независимо от возраста ребенка при значительном снижении уровня артериального давления, а также потери жидкости и солей, нарушается сознание.
Диагностика состояния
При определении функции надпочечников врач учитывает характерную клиническую картину, а также назначает обследование. В пользу аддисоновой болезни свидетельствуют такие нарушения:
- УЗИ надпочечных желез – туберкулезные очаги или отложения кальция (только при туберкулезной инфекции);
- анализ крови – антитела к 21-гидроксилазе, снижение кортизола, общего белка, глюкозы, натрия, лейкоцитов, повышен калий, лимфоциты и эозинофилы;
- анализ мочи – низкое выделение кортизола, 17-ОКС;
- КТ и МРТ гипофиза и гипоталамуса для исключения новообразования.
Наиболее информативно определение АКТГ в крови. При поражении надпочечных желез он повышен, а если причина в головном мозге – снижен. Если результат анализа крови оказался сомнительным, то АКТГ вводят извне.
Этот тест называется стимуляционным, так как при его помощи оценивают изменение выделения кортизола спустя 30 минут и час. Если его уровень вырос менее, чем на 530 нмоль/л, то диагноз гипокортицизма считается подтвержденным.
Чтобы доказать вторичный механизм появления патологии вводится инсулин. Он в норме стимулирует выделение АКТГ и кортизола в ответ, а при аддисоновой болезни этого не происходит.