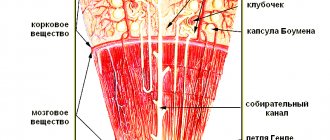
Элементарной функциональной единицей почек является нефрон, структура, которая непосредственно отвечает за фильтрацию плазмы крови. Важнейшим составляющим его функционирования является поддержание артериального давления у константных значений. За данный физиологический показатель отвечает юкстагломерулярный аппарат (ЮГА), непосредственно связанный с нефроном. Он является важнейшим регулятором артериального давления в организме, поддерживающим адекватное кровоснабжение почек.
Особенности строения почек
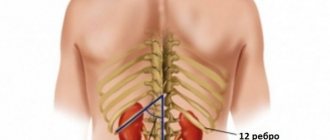
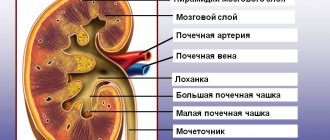
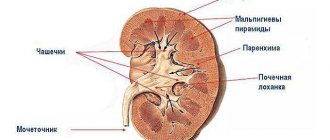
Почки — гормонально активные паренхиматозные парные органы мочевыделения. У человека наблюдается поясничное расположение почек, при котором органы связаны с аортой короткими ренальными артериями. Они обеспечивают обильное кровоснабжение, которое составляет 25 % от систолического выброса. Под влиянием артериального давления кровь проталкивается до мелких афферентных артериол, где попадает в капсулу клубочка и фильтруется.
Форменные элементы крови и некоторая часть ее плазмы отводятся по эфферентной артериоле, которая гораздо меньше афферентной по диаметру. Это необходимо для поддержания более высокого давления жидкости на входе, что поддерживает фильтрацию, обеспечивая лишь небольшой сброс в отводящую артериолу. Также регулятором давления является юкстагломерулярный аппарат почек. Он представляет собой совокупность клеток, непосредственно связанных с синтезом ренина и его регуляцией.
Ренин и ангиотензиноген
Попадая в кровь, ренин «встречается» с другим веществом, которое ученые назвали ангиотензиногеном.
Обычный ангиотензиноген находится в крови в спокойном, совершенно неактивном состоянии. И только встречаясь с ренином и контактируя с ним, ангиотензиноген превращается в ангиотензин I. Далее из ангиотензина I образуется биологически активное вещество ангиотензин II.
Ангиотензин II повышает тонус сосудов, что приводит к сужению их просвета и повышению давления крови в них. Но это еще не все. Ангиотензин II стимулирует выработку другого активного вещества — альдостерона.
Альдостерон же приводит к задержке воды в организме. Он увеличивает реабсорбцию или обратное всасывание воды в канальцах нефрона. Добытая таким образом вода поступает в сосуды, наполняя их и увеличивая артериальное давление.
Вот такое повышение артериального давления, которое вызывается гормоном почки ренином, принято называть почечным давлением.
Морфология ЮГА
Юкстагломерулярный аппарат состоит из трех типов клеток, расположенных в непосредственной близости от нефрона и образующих с ним функциональную систему с положительной обратной связью. Первый тип клеток — эпителиоидные (или зернистые), которые представляют собой видоизмененные гладкие миоциты мышечной стенки артериолы. Они в большом количестве располагаются в мышечном слое афферентной артериолы и в меньшем — в эфферентной. Это указывает на их причастность к определению разности гидростатического давления в этих сосудах.
В зернистых клетках имеются барорецепторы, которые передают информацию на юкставаскулярные клетки ЮГА. Зернистые клетки также являются основными производителями ренина, фермента, регулирующего артериальное давление в кровеносной системе. Этот фермент также частично способны синтезировать юкставаскулярные клетки (второй тип) юкстагломерулярного аппарата. Функции данных клеток сводятся к тому, что они являются связующим звеном между эпителиоцитами и плотным пятном мочевого канальца. Юкставаскулярные клетки располагаются в пространстве между афферентной и выносящей артериолой ЮГА.
А — схема мочеобразующей системы почки. Б — схема сосудистой системы почки
Каждая из двух почек получает артериальную кровь через артерию почек (A. renalis),
которая через междолевые артерии (Aa.
interlobares)
попадает в дуговые артерии (Aa.
arcuatae).
От них вертикально ответвляются в направлении поверхности почек междольковые артерии
(Aa. interlobulares),
от которых при прохождения через
корковое веществоотходят приносящие артериолы. Приносящая артериола (Vas afferens)
разветвляется в
клубочкена клубочковые капилляры (первая капиллярная сеть),которые выглядят как висящие на веточках яблоки. В отличие от кровоснабжения в других органах, капилляры клубочков не сразу переходят в венулы: клубочковые капилляры снова собираются вместе в выносящую артериолу (Vas efferens).
Выносящие артериолы клубочков, расположенных в поверхностных и средних слоях коркового вещества, снова разветвляются на
околоканальцевые капилляры.Они контактируют прежде всего с клетками дистальных канальцев, расположенных в корковом веществе почек (вторая капиллярная сеть). Кровоснабжение мозгового вещества почкиосуществляется не с помощью артерий, а с помощью выносящих артериол, выходящих из так называемых юкстамедулярных клубочков.
Строение нефрона
Почечная доля состоит из большого числа структурных единиц — нефронов.
Различают два типа нефронов — кортикальные (корковые) нефроны(~85%) и юкстамедулярные нефроны(~15%). Почечное тельце кортикального нефронарасположено в наружной части коркового вещества (внешняя кора) почки. Петля Генле (старая номенклатура, которую в редких случаях мы применяем для простоты изложения) у большинства кортикальных нефронов имеет небольшую длину и располагается в пределах внешнего мозгового вещества почки. Почечное тельце юкстамедулярного нефронарасположено в юкстамедулярной коре, около границы коры почки с мозговым веществом. Большинство юкстамедулярных нефронов имеют длинную петлю Генле. Их петля Генле проникает глубоко в мозговое вещество и иногда достигает верхушек пирамид.
Одна почка содержит около 1 млн клубочков, которые расположены большей частью в поверхностных слоях коркового вещества(клубочки поверхностных корковых нефронов),а часть их лежит близко к мозговому веществу (клубочки
юкстамедулярных нефронов).Клубочек вместе с капсулой Боумена с системой канальцев образует структурную и функциональную единицу почки — нефрон.У юкстамедулярных нефронов часть канальца, называемая петлей Генле, глубоко уходит во внутреннее мозговое вещество почки. Дистальный участок канальца вливается через связывающий каналец в собирательный проток.
В каждом нефроне (по новой номенклатуре) ясно различимы следующие отделы рис. 9-3:
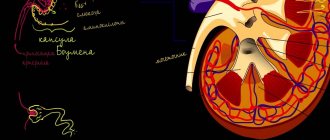
(1) капсула клубочка, capsula glomeruli (Bowmom)
— боуменова капсула в виде чаши, охватывающей клубочек артериальных капилляров
(glomerulus);
(2) проксимальный извитой каналец; (3) проксимальный прямой каналец; (4) нисходящий тонкий сегмент петли (тонкий нисходящий отдел петли Генле); (5) восходящий тонкий сегмент петли (тонкий восходящий отдел петли Генле); (6) дистальный прямой каналец (толстая восходящая часть петли Генле); (7) дистальный извитой каналец; (8) связующий каналец; (9) начальный отдел собирательного протока; (10) корковый собирательный проток; (11) наружный мозговой собирательный проток; (12) внутренний мозговой собирательный проток; (13) проток Беллини.
Рис. 9-3. Микроанатомия почки
Клубочек и околоклубочковый аппарат нефроза
На рис. 9-4 последовательно показано строение нефрона (рис. 9-4 А), дан переход к строению капсулы Боумена (рис. 9-4 Б) и к структуре фильтрационного барьера (рис. 9-4 В).
Клубочковый фильтрсостоит из трех слоев: фенестрированного эндотелия капилляров, базальной мембраны и расположенного со стороны нефрона эпителия с подоцитами. Между пальцевидными отростками подоцитов натянуты щелевидные мембраны с порами малого диаметра. В одном клубочке через этот фильтр фильтруется около 70 мкл в день, а в двух почках вместе взятых — 180 л в день (GFR).
Юкстагломерулярный,или околоклубочковый, аппаратявляется совокупностью клеток почки, регулирующей функции отдельного нефрона. Назван юкстагломерулярный аппарат так потому, что расположен вблизи клубочка, образуя треугольник: с двух сторон окружен афферентной и выходящей эфферентной артериолами, а с третьей — стенкой дистального извитого канальца. Такое расположение обеспечивает выполнение ключевых функций — регуляции потока почечной крови и уровня клубочковой фильтрации. Юкстагломерулярный аппарат (JGA) состоит из
трех основных частей — macula densa
(плотное пятно)
— область плотно упакованных призматических эпителиальных клеток дистального извитого канальца нефрона в области, прилегающей к почечному тельцу, юкстагломерулярныхи юкставаскулярных клеток.
Клетки macula densa чувствительны к ионному составу, а также к количеству воды в моче, вызывая синтез ренина остальными клетками юкстагломерулярного аппарата.
Юкстагломерулярные клетки(или, иначе, гранулярные клетки,расположенные в стенке приносящей артериолы, содержащие ренин. Ренин — неотъемлемая часть ренин-ангиотензинальдостероновой системы, регулирующей давление крови.
Юкставаскулярные клетки,или клетки Гурмагтига,— это клетки почки, расположенные между macula densa и приносящей артериолой. Эти клетки относятся к специализированным мезангиальным. Они имеют длинные отростки, контактирующие с остальными клетками. Юкставаскулярные клетки вырабатывают фермент ангиотензиназу, обусловливающий инактивацию ангиотензина, следовательно, является антагонистом деятельности ренин-ангиотензинового аппарата и способны вырабатывать ренин.
Рис. 9-4. Клубочковый фильтр и юкстагломерулярный аппарат
Канальцевый аппарат нефрона
Канальцы и собирательная трубочка выстланы клетками эпителия, в мембраны которых и со стороны просвета канальца (апикальная или люминальная мембрана), и со стороны интерстициального пространства и капилляров (базолатеральная мембрана) асимметрично встроены белковые структуры (насосы, переносчики и ионные каналы), обеспечивающие перенос веществ через мембраны путем активного (первичного и вторичного) транспорта, облегченной и простой диффузии. Это делает возможным направленный транспорт тех или иных соединений.
Проксимальный извитой каналец.Стенка проксимального извитого канальца (сегмент S1), выстлана высокими сцепленными друг с другом эпителиальными клетками, которые со стороны просвета канальца несут на себе щеточную каемку и на базальной мембране имеют глубокие складки (базальный лабиринт), что совместно увеличивает поверхность в 30-60 раз. Это свидетельствует о количественно высоких транспортных задачах проксимального канальца. Прилежащие к базальным складкам митохондрии обеспечивают работу Na+/К+-АТФазы базолатеральной мембраны АТФ. Кроме того клетки эпителия имеют контакты типа tight junction
и через эти плотные контакты между эпителиальными клетками (межклеточно) переносятся сравнительно большие количества растворенных веществ.
Высокая проницаемость проксимального канальца для воды лишь в некоторой мере объясняется «протеканием» его плотных контактов. Важнее то, что как в апикальную клеточную мембрану (со стороны просвета канальца), так и в базолатеральную мембрану (со стороны интерстициума) встроены водные каналы (AQP 1,аквапорин 1).
В целом, после многочисленных поворотов извитой части в корковом веществе почки проксимальный каналец спускается своей прямой частью во внешние слои мозгового вещества почки. Размер клеток, плотность и высота щеточной каемки, глубина базолатеральных складок, а также плотность митохондрий уменьшаются по ходу проксимального канальца, что отражает снижение количества транспортируемых веществ (путем реабсорбции)
в нижележащих отделах проксимального канальца. Различают (нечетко разделенные) сегменты S1 (или P1; большая часть извитого канальца) и S2, а также лежащий исключительно в мозговом веществе почки сегмент S3 (каналец — см. ниже).
Проксимальный прямой каналец.Стенка проксимального прямого канальца (сегмент S3), выслана эпителиальными клетками, но их характерные черты (описанные выше) уже не так сильно выражены. Однако прилежащие к базальным складкам митохондрии обеспечивают Na+/К+-АТФазу базолатеральной мембраны АТФ. Кроме того, эти клетки также имеют контакты типа tight junction
и через эти плотные контакты между ними (межклеточно) переносятся растворенные вещества.
Нисходящий тонкий сегмент петли (тонкий нисходящий отдел петли Генле).Клетки эпителия нисходящего тонкого сегмента лишены щеточной каемки, бедны митохондриями и обладают низким уровнем метаболической активности.
Восходящий тонкий сегмент петли (тонкий восходящий отдел петли Генле).Клетки эпителия восходящего тонкого сегмента аналогичны предыдущим, однако более уплощены. Они также лишены щеточной каемки, бедны митохондриями и обладают низким уровнем метаболической активности.
Дистальный прямой каналец (толстая восходящая часть петли Генле).Клетки эпителия этого отдела нефрона — крупные клетки, обладающие высокой метаболической активностью и способностью к активной реабсорбции.
Дистальный извитой каналец.Эпителиальные клетки этого отдела нефрона похожи на клетки дистального прямого канальца, но основное отличие связано с тем, что в дистальном извитом канальце представлено два типа клеток, которые различаются по структуре и функциям — это главные и вставочные клетки. Эти два типа клеток реабсорбируют и секретируют разные вещества.
Эпителиальные клетки связующего канальца, начального отдела собирательного протока, коркового собирательного протока, наружного мозгового собирательного протокаи внутреннего мозгового собирательного протокаимеют практически кубическую форму с гладкой поверхностью и содержат небольшое количество митохондрий. Они выполняют разные функции.
Рис. 9-5. Строение трубочек по длине нефрона
Определение фильтрационной способности почек
Скорость клубочковой фильтрации,равная 120 мл/мин, является важнейшей константой организма. Фильтрация загружает работой весь нефрон. Любые изменения фильтрации приведут к изменению работы всех отделов нефрона. Скорость фильтрации оценивают по клиренсу. Клиренс вещества— скорость, с которой объем плазмы полностью очищается от данного вещества почками в единицу времени.
Высокая скорость клубочковой фильтрации (т.е. объем фильтрата, образующийся в единицу времени; GFR: glomerular filtration rate)
является решающей для нормальной функции почек. Обычно
GFR составляет 85-135 мл/мин на каждые 1,73 м2 поверхности тела.Многие заболевания почек опасны из-за того, что они приводят к значительному снижению величины GFR. Поэтому измерение GFR становится главной задачей, когда необходимо оценить работу почек. Как же можно измерить у пациентов скорость протекающей внутрипочечной фильтрации?
В соответствии с правилом, введенным в обиход А. Фиком, с помощью растворенного в плазме крови вещества-индикатора, концентрация которого измеряется на входе (артерия) и на выходе (вена) любого органа, можно рассчитать объемную скорость плазматока через данный орган. Существуют три способа, с помощью которых может быть увеличено количество определенного вещества в просвете нефрона — это фильтрация, секрецияи метаболический синтез.Также существует три возможности снижения количества вещества в просвете нефрона: реабсорбция, экскреция и метаболическое расщепление.Если в крови циркулирует вещество, например полисахарид инулин,который свободно фильтруется, не реабсорбируется, не секретируется, не синтезируется и не расщепляется в просвете нефрона, то он может попасть в просвет почечных канальцев лишь в результате фильтрации и может быть выведен из организма только с мочой. В результате, справедливо утверждение: профильтрованное количество инулина / время = выведенное с мочой количество инулина / время (1).
Так как (количество вещества в растворе / время) = (объем раствора / время), то концентрация вещества, а кроме того концентрация свободно фильтруемого вещества, такого как инулин, в плазме крови и фильтрате практически равны (Pin [г/л]), уравнение (1) может быть записано в следующем виде:
где GFR измеряется в мл/мин, Vu — скорость образования мочи (мл/мин) и Uin — концентрация инулина в конечной моче (г/л). На практике инулин вводится в организм, а затем измеряется его концентрация (например, фотометрически) в плазме крови и моче. Для определения Vu сначала опорожняется мочевой пузырь (эта моча не берется в расчет: объем = 0; время = 0), после чего собирается моча в течение длительного (12-24 ч) периода времени. Разделив собранное количество мочи на время, прошедшее с момента первичного опорожнения мочевого пузыря, получают Vu. С помощью правила Фикаможно напрямую рассчитать величину GFR, используя преобразованное уравнение (2):
где GFR — скорость клубочковой фильтрации, Vu — скорость образования мочи (мл/мин), Uin — концентрация инулина в конечной моче (г/л), Pin — концентрация инулина в плазме крови (г/л).
Правая часть уравнения (3) называется клиренсом,и, таким образом: клиренс инулина (Cin) = GFR. Поскольку инфузия инулина является трудоемким методом, клиренс инулина определяется лишь в исключительных случаях. Проще проводить измерение GFR с помощью индикатора, который обычно находится в плазме крови, — креатинина. Он образуется из фосфокреатина в процессе обмена веществ в мышцах. Эндогенный креатинин не столь строго как инулин соответствует вышеназванным критериям (в том числе отсутствию секреции), но при этом определение клиренса эндогенного креатинавполне достаточно для рутинной проверки фильтрационной способности почек.
Для расчетов можно также использовать метод баланса массы (рис. 9-6). Поскольку вход вещества Х равен выходу Х,
где PX,a и PX,v — концентрация вещества Х в плазме почечной артерии и почечной вены соответственно. RPFa и RPFv — скорость артериального и венозного тока плазмы в почке. Ux — концентрация вещества Х в моче.
На основании этого рассчитывается классическое уравнение клиренса:
Рис. 9-6. Клиренс
Фильтрационный барьер нефрона
Эндотелий капилляров, базальная мембрана и отростки подоцитов образуют фильтр. В узком смысле понятие клубочекохватывает лишь сеть капилляров между приносящей и выносящей артериолами. Вместе с боуменовой капсулой он образует почечное тельце (рис. 9-7 А) диаметром 0,2 мм. На рис. 9-7 А структура клубочка схематично показана на срезе. Приток крови к капиллярным петлям (подключенным параллельно) обеспечивается за счет приносящей артериолы, а отток — выносящей артериолы. Между входящей в клубочек приносящей артериолой и выходящей из него выносящей артериолой лежат клетки мезангиума, к которым прижимается область Macula densa
дистального канальца этого же нефрона. Капиллярное переплетение вдается во внутреннее пространство боуменовой капсулы, проксимальный каналец начинается на противоположной стороне боуменовой капсулы. Пространство боуменовой капсулы отделяется от просвета капилляра
трехслойным фильтрационным барьером(рис. 9-7 Б). Его образуют: эндотелийкапилляров клубочков, целостность которого прерывается порамис диаметром в 50-100 нм; трехслойная базальная мембрана,в которой в качестве фильтра служит сеть из коллагена IV, ламинина и нидогена, в которую встроены отрицательно заряженые глюкозаминогликаны (анионный барьер), и наконец, «висцеральный» листок эпителия боуменовой капсулы.
Висцеральный листок в разрезе прерывист, так как отростки эпителиальных клеток (подоцитов)переплетаются друг с другом, при этом между отростками остаются свободные щели. При более сильном увеличении можно увидеть, что эти щели перекрыты щелевидной мембраной и имеют отверстия величиной лишь около 4×14 нм. Щелевидная мембрана содержит важный для проницаемости фильтра протеин, нефрин,который заякорен через другой протеин, CD2AP,на соседних отростках подоцитов. Торчащие с обеих сторон в щель молекулы нефрина скрепляются друг с другом на подобии застежки молнии и оставляют между собой свободными щелевые поры,которые едва пропускают молекулы альбумина.
Клетки крови задерживаются уже первым слоем фильтра — эндотелием. Это справедливо и для больших белковых молекул, поскольку in vivo
поры эндотелия вероятно покрыты отрицательно заряженным слоем белков. Способность к фильтрации макромолекул (молекулярная масса которых
около 10 000-70 000 Da) через следующие два слоя определяются не только шириной пор компонентов фильтра, но также и электрическим зарядом структур поверхностей фильтра.
Очищение фильтраобеспечивается клетками мезангиума и подоцитами клубочка, которые способны удалять высокомолекулярные отложения за счет фагоцитоза и последующего переваривания в лизосомах. При патологии масса отложений возрастает (например, комплексов антиген-антитело) клетки мезангиума начинают усиленно делиться. Это приводит к тому, что из-за ограниченного пространства капилляры сжимаются и количество фильтрата снижается.
В клубочке образуется ультрафильтрат,который наряду с водой содержит только небольшие молекулы. Свободно фильтруются лишь молекулы малого размера, радиус которых меньше 1,6-1,8 нм. Это соответствует молекулярной массе 6 000- 15 000 Da. Инулин, который используется для определения клиренса, имеет молекулярную массу около 5 000 Da и относится к данной группе. Для глобулинов радиусом >4,4 нм (> 80 kDa) фильтр обычно непроницаем, тоже самое справедливо и для эритроцитов, обладающих еще большими размерами. Вещества, радиусы молекул которых находятся в этих границах, фильтруются лишь частично: миоглобин (17 000 Da) на 75% и альбумин (69 000 Da) лишь на 0,03%. Плохо фильтруются также низкомолекулярные вещества, связанные с белкамиплазмы крови. Ca2+, например, фильтруется лишь на 60% вследствие того, что около 40% Ca2+ связывано с белками плазмы крови. Многие медикаменты, например большинство сульфаниламидов или сердечный гликозид дигитоксин, еще в большей степени связаны с белками плазмы крови, поэтому они крайне медленно выводятся почками.
Проницаемость фильтра для макромолекул с радиусом <4,4 нм зависит от заряда молекулы(рис. 9-7 Б). Причиной тому является отрицательный заряд структур поверхностей фильтра, за который ответственны анионные глико(сиало)- протеины. Они расположены на структурах базальной мембраны (как со стороны капилляра, так и со стороны боуменовой капсулы), а кроме того на поверхности внешней мембраны отростков подоцитов. Этот факт важен с точки зрения патофизиологии, поскольку уменьшение заряда структуры поверхностей фильтра резко повышает фильтрацию альбумина (рис. 9-7 В), что приводит к потерям большого количества этого белка плазмы крови с мочой — альбуминурия.
Рис. 9-7. Макро- и микроструктура фильтра капсулы Боумена (А). Зависимость проницаемости фильтра от заряда молекулы (Б, В)
Движущая сила фильтрации в нефроне
Эффективное фильтрационное давлениеявляется движущей силой фильтрации, причем давление крови в клубочковых капиллярах является его значительной составной частью. Процесс фильтрациисам по себе хотя и является пассивным процессом,однако для поддержания градиента давления должна постоянно затрачиваться энергия. Это происходит вдали от почек: в сердце, где АТФ потребляется для сокращения желудочка сердца, обеспечивающего давление крови.
По пути к капиллярам клубочков давление крови падает до уровеня 48 мм рт.ст. (Ркап; рис. 9-8 А). Однако оно не может быть полностью использовано для фильтрации, поскольку ему противодействуют два других давления. С одной стороны — это давление в боуменовой капсуле (РБоум) величиной около 13 мм рт.ст. Вычитание РБоум из Ркап дает гидравлическую разницу давлений(ΔΡ)величиной 35 мм рт.ст. С другой стороны, белки плазмы практически не проходят через фильтр, что обуславливает коллоидоосмотическое (онкотическое) давление крови(πкап), которое действует против ΔΡ. В плазме πкап составляет в среднем примерно 25 мм рт.ст. (Онкотическое давление в фильтрате не принимается в расчет, поскольку он практически не содержит макромолекул, отсюда и происходит название «ультрафильтрат»). Итак, эффективное фильтрационное давление (Рэфф) рассчитывается следующим образом:
Это значение, измеренное у крысы (у человека оно не должно сильно отличаться), превалирует на приносящем конце клубочкового капилляра. По ходу капилляра значительно изменяется не
Ркап, а πкап. Это связано с тем, что во время про-
хождения по капилляру из плазмы в процессе фильтрации постоянно удаляется вода. В результате πкапвозрастаетнелинейно и достигает в капилляре при 20%-м удалении воды (фильтрационная фракция) значений около 35 мм рт.ст. Рэфф снижается до 0 (рис. 9-8 А), и фильтрация прекращается. Если эта точка достигается еще до конца капилляра клубочка, то данное фильтрационное равновесиеограничивает фильтрацию (рис. 9-8 Б). Если же в этом случае увеличивается почечный кровоток, то место фильтрационного равновесия сдвигается в конец капилляра, так что используется большая фильтрационная поверхность. Это может быть причиной зависимости GFR от почечного кровотока.
Итак, для нормальной GFR необходимы не только нормально функционирующие клубочки (поверхность фильтра, гидравлическая прницаемость, количество), но также:
— нормальное капиллярное давления Ркап;
— нормальный состав белков и их концентрация и, тем самым, нормальное онкотическое давление плазмы (πкапк);
— нормальное давление в пространстве боуменовой капсулы (РБоум).
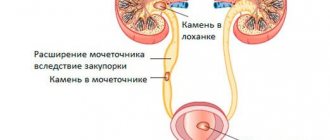
Поэтому изменения в GFRмогут быть вызваны колебаниями трех вышеназванных давлений. Так GFR снижается, например, при падении среднего системного давления крови ниже 75 мм рт.ст., при шоке (снижается Ркап), при патологически повышенной концентрации белков в плазме (множественная миелома; повышается πкап), или когда препятствие в мочевыводящих путях (опухоль или почечный камень) затрудняет отток мочи (повышается РБоум). Наоборот, GFR повышается, когда поднимается Ркап (например, при гипертонии со значениями давления крови за пределами ауторегуляторной области), или когда снижается πкап (при гипоальбуминемии в результате недоедания).
Рис. 9-8. Эффективное фильтрационное давление (Рэфф). Рэфф — движущая сила фильтрации.
равно давлению в капиллярах минус онкотическое давление в плазме πкап) и давление в Боуменовой капсуле (PБоум).Поскольку отток воды из плазмы (фильтрационная фракция — 0,2=20%) увеличивает концентрацию белков в плазме и повышает тем самым по ходу капилляров, уменьшается и даже может достичь нулевого значения (фильтрационное равновесие; А). Произведение среднего эффективного фильтрационного давления проницаемости фильтра для воды и его поверхности (два последних множителя вместе дают Kf) соответствует скорости клубочковой фильтрации одного клубочка (Б). Если фильтрационное равновесие сдвигается в конец капилляра, как это происходит в случае усиления почечного кровотока, то может быть использована большая поверхность фильтра, и GFR возрастает
Механизмы реабсорбции Na+ и Cl-
Проксимальные канальцы могут реабсорбировать ионы, например, Na+ и Cl- двумя путями — через клетку (трансклеточным:transcellular)
и
межклеточным (параклеточным:paracellular)
способом, как это показано в виде принципиальной схемы путей на рис. 9-9 А.
При трансклеточном путиNa+ и Cl- последовательно пресекают апикальную и базолатеральную мембраны до поступления в кровь. При параклеточномпути эти ионы двигаются полностью внеклеточным путем через tight junction
между соседними клетками.
При трансклеточном пути скорость транспорта зависит от электрохимического градиента, наличия ионных каналов и транспортеров на апикальной и базолатеральной мембране. При параклеточном пути трансэпителиальные электрохимические движущие силы и проницаемость tight junctions
определяет движение ионов.
Основной механизм трансклеточной реабсорбции Na+ одинаков во всех сегментах нефрона и представляет собой различные варианты классического эпителиального транспорта в условиях модели, включающей две мембраны (рис. 9-9 Б). Первая ступеньв этой модели — пассивный вход Na+ в клетку через апикальную мембрану.Поскольку внутриклеточная концентрация Na+ мала и потенциал клетки негативный по сравнению с канальцем, электрохимический градиент благосклонен для пассивного входа Na+ через апикальную мембрану. Однако различные сегменты канальцев используют различные механизмы для пассивного входа Na+ через апикальную мембрану.
Вторая ступеньв этой модели трансклеточной реабсорбции — активное «выталкивание» Na+ из клетки через базолатеральную мембрану.Na+/К+-АТФаза, расположенная на базолатеральной мембране (первично-активный транспорт), играет основную роль в этом процессе.
Рис. 9-9. Трансклеточные и межклеточные пути реабсорбции на примере Na+ и Cl-
Реабсорбция Na+ в различных частях нефрона
В проксимальном извитом канальце(рис. 9-10 А) Na+ переходит из просвета канальца в клетки по его электрохимическому градиенту с помощью белков-переносчиков, которые одновременно переносят в клетки глюкозу (рис. 9-10 А), а также аминокислоты, фосфат и т.д. (котранспорт). Кроме того, в процессах переноса Na+ в клетки участвует также Na+-Н+-переносчик (антипорт), работа которого способствует в данном случае реабсорбции профильтрованного бикарбоната (рис. 9-10 А). Большинство переносчиков (котранспорт) электрогенны, поэтому развивается трансэпителиальный потенциал более отрицательный в просвете канальца. Благодаря ему в нижележащих сегментах канальца межклеточно реабсорбируются ионы Cl-. В результате реабсорбции любого вещества устанавливается осмотическая разница между просветом канальца и интерстициальной жидкости, осмотическое давление которой увеличивается, что ведет к оттоку воды из просвета канальца по осмотическому градиенту. Вода увлекает за собой растворенные в ней вещества (перенос вместе с растворителем или solvent drag),
что является еще одной формой пассивного транспорта веществ.
В целом реабсорбция Na+ в проксимальном извитом канальце может осуществляться (1) посредством (электронейтрального) Na+-H+-переносчика (антипорт),таким образом на каждый реабсорбируемый ион Na+ в просвет канальца выделяется в результате вторичного активного транспорта ион Н+, который в этом отделе участвует в сложном механизме реабсорбции бикарбоната HCO3-; (2) посредством целого ряда переносчиков Na+,которые помимо Na+ присоединяют и переносят в клетку в результате вторично-активного транспорта D-глюкозу, нейтральные или кислые аминокислоты, фосфат, сульфат, галактозу, витамин С, лактат, ацетат, цитрат, ацетоацетат, сукцинат или другие вещества (котранспорт).В этом случае Na+ движется в клетку по электрохимическому градиенту, а названные вещества идут против их электрохимических градиентов.
Проникновение Na+ в клетку при этом является процессом пассивным. Энергия высокого электрохимического градиента Na+, созданного Na+/К+-АТФазой, используется также для того, чтобы названные в пункте (1) ионы Н+ в результате вторичного активного транспорта были секретированы в просвет канальца в обмен на ионы Na+ (антипорт) и названные в пункте (2) вещества
реабсорбировались в результате вторичного активного транспорта, обусловленного работой белковпереносчиков, связывающихся одновременно с Na+ и этими веществами (котранспорт). Некоторые белки-переносчики могут связывать более одного иона Na+ и одновременно несколько других, переносимых веществ. В результате увеличивается движущая сила транспорта для веществ, переносимых с помощью вторичного активного транспорта: в случает двух ионов Na+ — в 2 раза (котранспорт).
В дистальном прямом канальце (толстой восходящей части петли Генле)процесс реабсорбции осуществляется с помощью белка-переносчика (вторичный активный транспорт, котранспорт), расположенного на апикальной мембране клеток эпителия. Он переносит одновременно 1Na+, 1К+ и 2Cl-, при этом движущей силой является градиент Na+ опять создаваемый Na+/К+-АТФазой, расположенной на базолатеральной мембране (первично-активный транспорт, рис. 9-10 Б). Через каналы на люминальной мембране К+ диффундирует обратно в просвет канальца (процесс рециркуляции). Диффузия К+ из клетки приводит к гиперполяризации люминальной мембраны. Кроме того, наличие ионов К+ в просвете канальца устанавливает трансэпителиальный потенциал, при котором жидкость в просвете канальца по отношению к интерстициальной жидкости заряжена положительно. Под влиянием этого трансэпителиального потенциала Na+ (и ряд других катионов) может быть реабсорбирован пассивно через проницаемые для катионов плотные контакты.
В дистальном извитом канальцереабсорбция Na+ продолжается вместе с Cl- (рис. 9-10 В). Оба этих иона из просвета канальца попадает в клетки дистального извитого канальца посредством механизма вторичного активного транспорта, обуславливающий одновременный перенос Na+ и Cl- (котранспорт; белок-переносчик: TSC). NaCl входит в клетку через апикальную мембрану посредством локализованного на люминальной мембране переносчика Na+ и Cl- (котранспорт), при этом Na+/К+-АТФаза на базолатеральной мембране активно выводит Na+ из клетки, поддерживая электрохимический градиент, обеспечивающий вход Na+ через люминальную мембрану. Работа этого электронейтрального Na+-Cl—переносчика стимулируется альдостероном, и тормозится диуретиком тиацидом. Поэтому он был назван TSC(thiazid-sensitive co-transporter).
Cl- выходит из клетки через Cl—каналы (тип CLC-Kb).
В корковом собирательном протоке(рис. 9-10 Г) в главные клетки Na+ попадает через Na+-каналы.
Рис. 9-10. Клеточные модели реабсорбции Na+ в различных участках нефрона.
⇐ Предыдущая15Следующая ⇒
Плотное пятно ЮГА
Третий тип клеток юкстагломерулярного аппарата — клетки плотного пятна, расположенного в дистальных участках мочевого канальца нефрона. Эти компоненты ЮГА несут на себе осморецепторы, посредством которых способны определять натриевую концентрацию. Они отслеживают изменения содержания натриевых ионов в уже отфильтрованной моче, из которой реабсорбировались питательные вещества и жидкость. В зависимости от значений концентрации, клетки плотного пятна передают информацию на юкставаскулярные клетки.
Последние обрабатывают сигнал и регулируют функцию эпителиоцитов. Эти зернистые клетки на основании полученной информации выделяют некое количество фермента ренина, чтобы влиять на показатель артериального давления. Таким образом ЮГА является той структурой, которая непосредственно на месте участвует в скорости фильтрации мочи. Вместе с нефроном они образуют целостную функциональную систему, поддерживающую жизнедеятельность организма человека.
Строение юкстагломерулярных клеток
Расположенные в почках клетки юкстагломерулярного аппарата имеют особое строение. Эпителиоциты ЮГА представляют собой видоизмененные гладкомышечные клетки, имеющие уплощенную форму. Их ядро многоугольное, а органеллы представлены в небольшом количестве. Их задачей является синтез фермента ренина, а потому аппарат биосинтеза в эпителиоцитах, которые также называются зернистыми клетками, сильно развит. При этом зерна в цитоплазме являются плазматическими цистернами с образованным ренином.
Особенности регуляции артериального давления
Юкстагломерулярный аппарат является примером гормонально активной структуры, которая имеет входные данные в виде артериального давления и способность влиять на него посредством синтеза ренина. Причем эффективность контроля за артериальным давлением напрямую зависит от количества жидкости в организме и состояния артериальных сосудов. В условиях ишемии, когда атеросклеротическое сужение артерий наблюдается в основных органах-мишенях человеческого тела, ЮГА обеспечивает повышение значений давления с целью поддержания достаточной скорости фильтрации в клубочках.
Эта функция не зависит от того, сколько почек у человека, так как она регулируется самыми сильными ферментными системами. Но в случае развития артериальной гипертензии эффективность фильтрации из-за более высокого давления (выше 120 mmHg) не увеличивается пропорционально росту АД. Она наиболее эффективна при давлении в 120-140 mmHg. А в случае увеличения показателя АД возникает риск повреждения клубочков, из-за чего юкстагломерулярный аппарат прекращает или снижает синтез ренина.
Почему повышается давление?
Все дело в том, что при многих заболеваниях почек страдает местное кровообращение. Страдают сосуды больной почки.
А это приводит к активации юкстагломерулярного аппарата, что, в свою очередь, приводит к повышению артериального давления во всем организме. То есть — к почечному давлению.
Теперь вы понимаете, почему при заболеваниях почек так часто возникает гипертония? Теперь вы понимаете почему, обнаружив у пациента высокие цифры артериального давления, доктор назначает обследование почек?
Ведь в целом ряде случаев, вылечив почки, можно избавить пациента от высокого почечного давления!
Почечное давление — это очень стойкое повышение артериального давления, которое плохо снижается обычными препаратами. А все потому, что снизить такое давление можно только тогда, когда будет устранена причина, вызвавшая его. Тоесть — будет восстановлено нормальное кровообращение в почках.
Влияние АД на функции ЮГА и почек
Длительное повышение АД приводит к смещению равновесия и разбалансировке ангиотензиновой системы и ЮГА. Это значит, что на фоне сужения почечных артерий из-за атеросклероза и на фоне последующего развития АГ происходит увеличение выработки ренина. Однако из-за фиброза артерий эффективность работы ангиотензинового механизма невелика: он приводит к росту давления, однако в приводящей артериоле оно не растет. Таким образом объясняется, как расположение почек и ЮГА влияет на все кровообращение и его регуляцию. Помимо этого гипертензия приводит к нефросклерозу — постепенной гибели нефронов почек, из-за чего АГ часто является предпосылкой почечной недостаточности. Тогда, независимо от того, сколько почек у человека, отмечается заметное снижение скорости фильтрации и эффективности почечных функций.